2023-04-06


本期内容摘自《临床试验前沿设计实操训练营》
《临床试验前沿设计实操训练营》模块二:一期临床试验设计,授课导师是来自美国安德森癌症中心的终身讲席教授袁鹰教授(波音设计原创发明人),课程受到了学员们的高度好评,同时我们也收到了学员们的很多问题,袁教授针对这些问题,做了两节答疑课(120分钟)。
第一题 课程案例中,解释了3+3设计探索MTD,计算了95%CI,请问置信区间95%是怎么计算出来的?
第二题 CRM最大样本量"N"怎么设置?
第三题 CRM设计也是3个3个的入组患者,和改良的3+3有什么不同?
第四题 课程中,袁教授演示CRM操作举例图像时,默认剂量与药物暴露成比例(线性),如果药物不成比例(或非线性),是不是CRM就不适用了?这个时候推荐用什么方法?
第五题 如果某个剂量下(比如已经爬到3~4个剂量组),因为疾病罕见的原因(导致)入组困难,在录入2个受试者的时候,迟迟无法入组,那么,可以根据决策表进行决定吗?
Q1: 将MTD推荐为25%,是否主要基于美国FDA的考虑?
Q2: 如果在美国申请IND,采用30%的目标MTD,一般会有什么影响?
Q3:25%的目标MTD是否可以外推到美国以外?例如如果在美国以外的地方采用BOIN,是否需要调整目标MTD?如:30%左右?
第七题 当一个剂量级别完成后,通常会召开SRC(safety review committee)会议,决定剂量d 递增或者递减,但是当入组3例患者后发生1例DLT,决策表提示要继续入组,需要获得SRC的同意,才能继续入组3例患者吗?
第九题 BOIN设计中,3例DLT可评估患者脱落1例的话,是否需要替换?还是只根据2例DLT可评估患者即可作出判断?
第十题 对于BOIN可以比较高效的探索到MTD/RP2D的方法,剂量扩展阶段是否需要持续观察毒性?例如贝叶斯后验毒性等,如果进行后验毒性监测的话,一般后验毒性改率如何设置?和BOIN保持一致(即25%)吗?后验毒性的定义是什么?与一期剂量爬坡毒性判断标准保持一致(符合DLT定义),还是规定≥3/4级毒性?
第十一题 如果剂量扩展阶段检测到毒性比估计的(如25%)更高,该如何处理?
第十二题 BOIN入组具有灵活性,不一定非要3+3的模式,可以每组1、2、3个患者,但这些都需要提前在方案中定义清楚吗?
第十三题 出于综合考虑,对假设的6个剂量组计划先2+2+2入组,之后再3+3+3入组,请问基于BOIN目前的设计是否能直接实现?还是需要重写代码?对于此种设计,基于您对FDA的了解,FDA是否会接受这种设计?
第十四题 目前一期研究也有看到使用i3+3(interval3+3设计),看起来和波音很类似,也有决策表,两者有哪些区别?各有哪些优缺点?
第十五题 波音设计和i3+3设计,国内外的接受度如何?
第十六题 为什么使用队列为3时,BOIN软件产生的决策表显示3,6,9以外的边界值?
第十七题 为什么BOIN的剂量升降边界值不随样本量变化?
第十九题 请教袁教授,BOIN设计软件里面,每个剂量组最大样本量(当时是12),这个12的确定有什么计算方式?不同的数字会有差别吗?对探索MTD有多大影响?(刚才老师提到一般最小是9)。
第二十题 案例中使用3+3设计,第二,第三个剂量为什么是8个,不是9个?

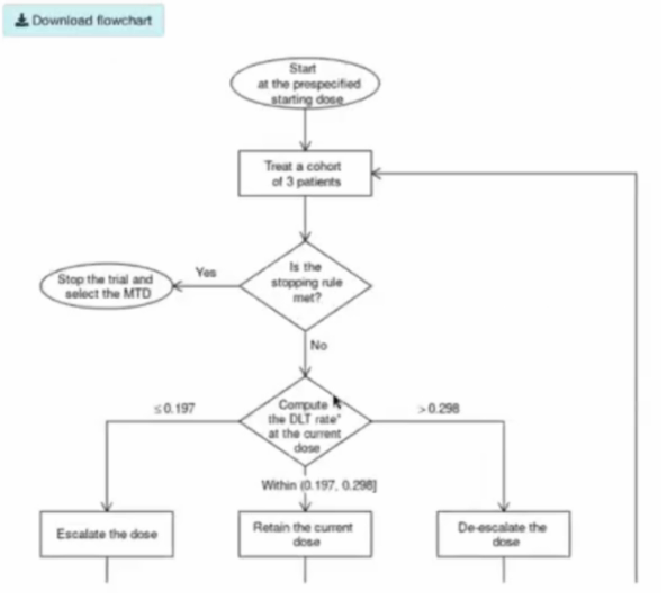
第二十一题 请教袁鹰教授关于BOIN设计的决策表和流程图看起来有些矛盾的问题,当入组3例患者,有1例DLT,计算的发生率是33%,按照流程图,找过29.8%应该要降一个剂量,但是按照决策图,是要保持在原剂量再入组3例的,看起来两者有些不一致,请教授解释一下。

一期临床试验设计(答疑课)
答疑导师:
袁鹰教授(美国安德森癌症中心)
答疑时长:120mins
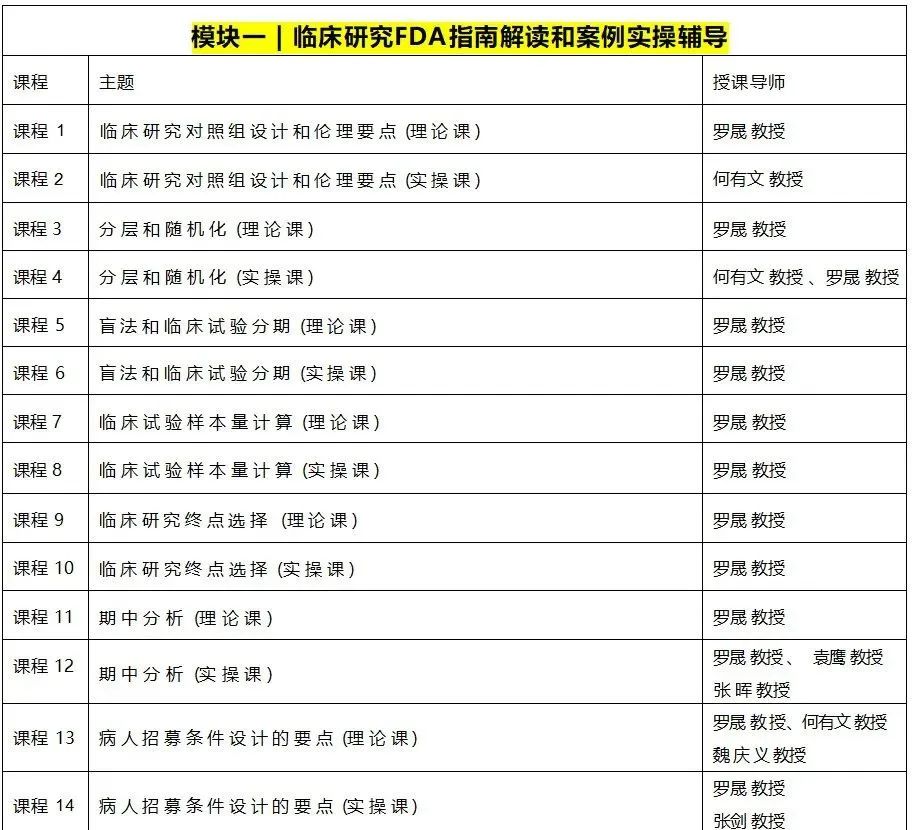
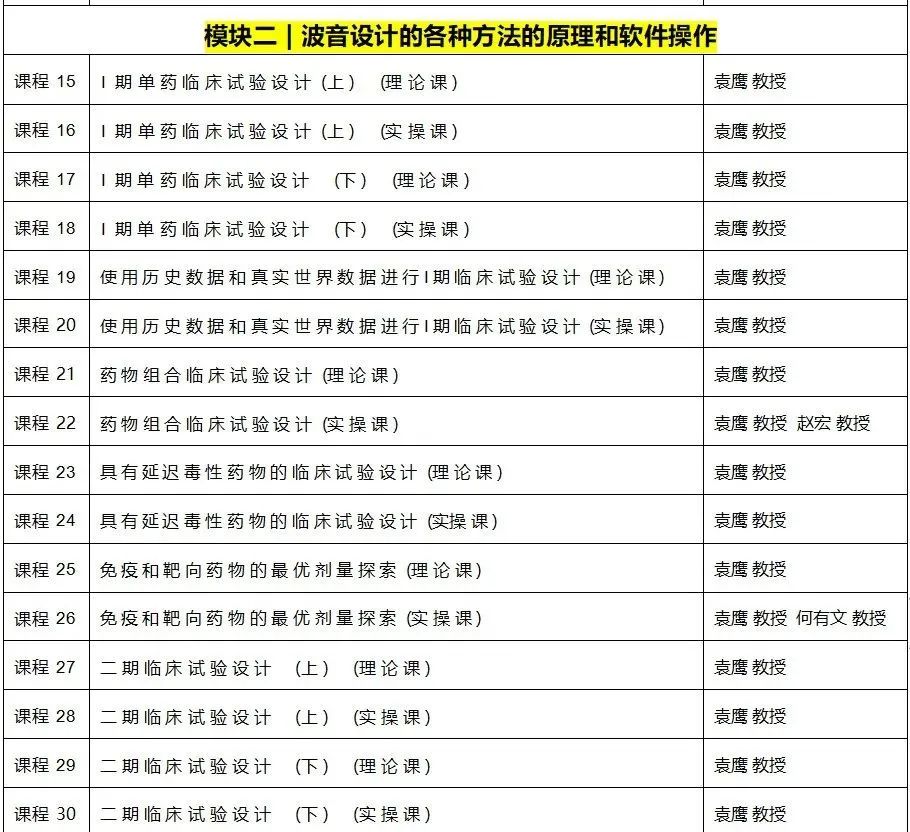
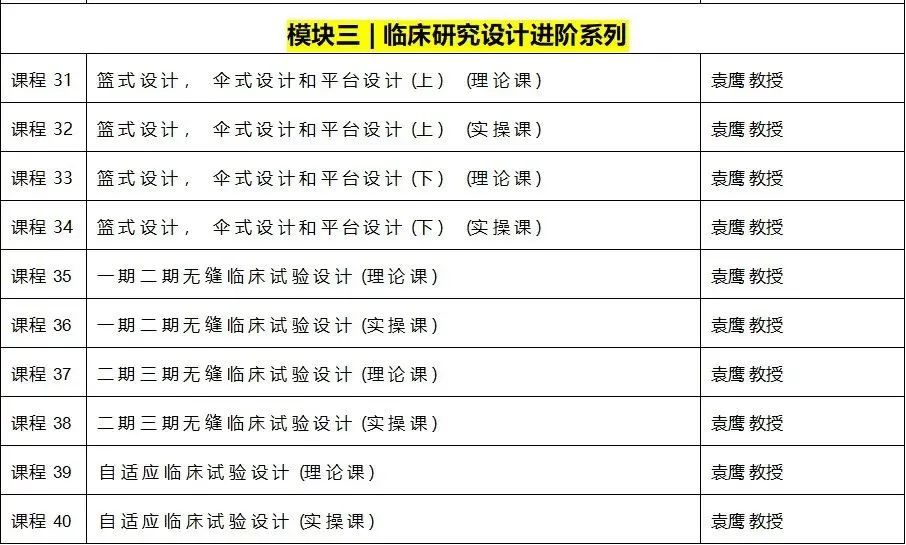
《临床试验前沿设计实操训练营》课程大纲
训练营导师简介




添加小编微信

百度浏览 来源 : 国际临研
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。




发表评论
注册或登后即可发表评论
登录注册
全部评论(0)