2022-08-29 来源 : 威斯腾生命科学研究院
2019年12月以来,一种新型冠状病毒SARS-CoV-2在全球迅速传播,引发全球公共卫生紧急事件。针对这种病毒的疫苗和抗病毒药物的缺乏带来了对小动物模型的迫切需求,而人血管紧张素转换酶II (ACE2)已被确定为SARS-CoV-2功能受体,中国食品药品检定研究员的王佑春等科学家利用CRISPR/Cas9敲入技术,将小鼠内源性ACE2 (mACE2)替换为hACE2,生成了稳定表达人ACE2的小鼠模型,此项研究于2020年7月发表在知名杂志《Cell Host & Microbe》上,文章题目为“A Mouse Model of SARS-CoV-2 Infection and Pathogenesis”,该研究生成的动物模型为研究SARS-CoV-2传播和发病机制以及评估COVID-19疫苗和治疗方法提供了一个有用的工具。

文章亮点
1.使用CRISPR / Cas9技术将人类ACE2(血管紧张素转化酶2)敲入小鼠体内
2. SARS-CoV-2会在肺、气管和大脑中大量复制
3. SARS-CoV-2引起老年hACE2小鼠间质性肺炎和细胞因子升高
4. 高剂量SARS-CoV-2可在hACE2小鼠胃内引起感染
研究结果
研究人员首先将hACE2的完整cDNA插入到小鼠体内位于x染色体上的GRC m38.p6位点的mACE2基因的第一个编码外显子Exon2 (图1)中,从而沉默mACE2基因,终止其表达,使得小鼠只表达hACE2而不表达mACE2,生成稳定表达hACE2的纯合子小鼠模型,并将其命名为hACE2- KI /NIFDC小鼠(简称hACE2小鼠)。
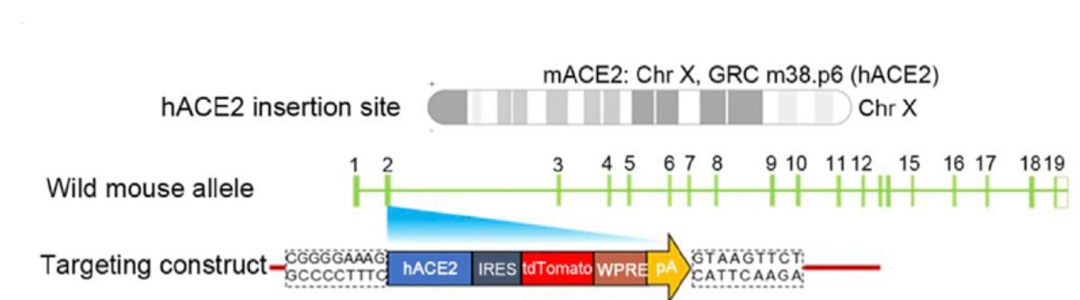
图1.将hACE2基因插入位于X染色体上的GRC m38.p6位点,小鼠ACE2的第一个编码外显子Exon2上
然后,为了进一步研究hACE2小鼠感染SARS-CoV-2的能力,用4 * 105 PFU 的SARS-CoV-2鼻内感染青年(4.5周龄)和老年(30周龄)hACE2小鼠,以接受相同病毒量的WT C57BL/6小鼠为对照组(图2A)。每天监测所有小鼠的临床症状和体重变化,并在感染后的第6天杀死小鼠。结果表明,接种后的小鼠均未出现明显的临床症状,只有老龄hACE2小鼠在接种第三天时体重下降10%,随后恢复。在年轻和年老的hACE2小鼠的肺、气管和脑组织中都可以看到病毒RNA复制旺盛,而在脾脏、肾脏、肝脏、肠道和血清中则没有检测到病毒(图2B);在野生型C57BL / 6小鼠的任何组织或血清中没有检测到病毒RNA。另外,研究人员还在老年hACE2小鼠的粪便中检测到高水平的病毒RNA(2.9* 105 copies/g)。通过对小鼠肺切片进一步免疫染色,发现青年、老年hACE2小鼠气道均检测到了病毒S蛋白,而在接种SARS-CoV-2的WT小鼠气道未能检测到病毒S蛋白(图2C)。为了确定模型中SARS-CoV-2的主要靶细胞,研究人员进一步用不同的细胞标记对感染hACE2小鼠的肺切片进行了染色,染色结果表明CC10+ Clara细胞是模型中SARS-CoV-2沿气道的主要靶细胞(图2D)。这些结果表明,与野生型小鼠相比,hACE2小鼠对SARS-CoV-2的鼻内感染高度敏感,病毒RNA在肺Clara细胞、气管和大脑中复制旺盛。
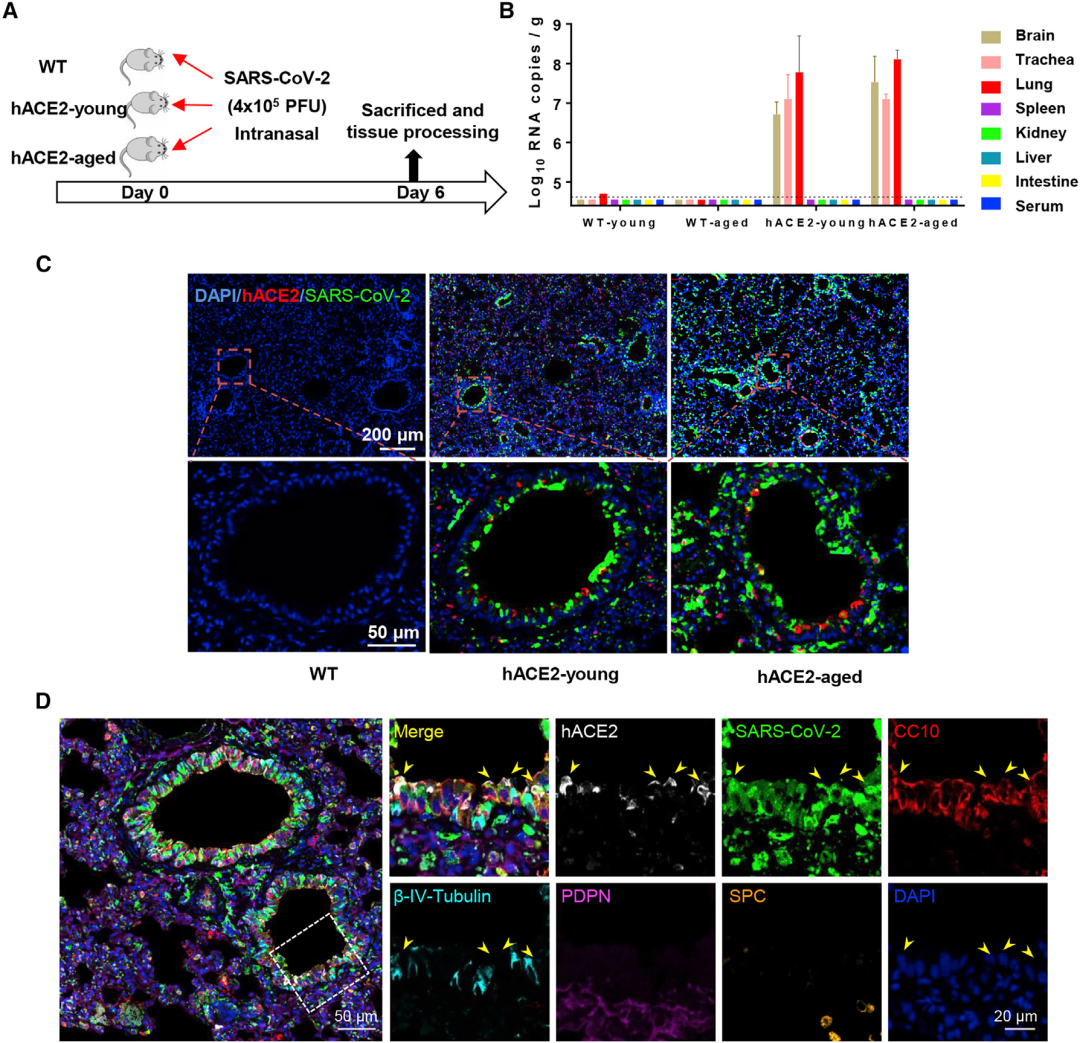
图2. A. 用4×105 PFU的SARS-CoV-2病毒鼻内感染WT C57BL/6小鼠,青年(4.5周龄)和老年(30周龄)的hACE2小鼠(n = 3) ,并在接种后第六天杀死小鼠收集组织;B. SARS-CoV-2病毒RNA的组织分布;C. 小鼠肺石蜡切片免疫荧光染色,SARS-CoV-2 S蛋白(绿色),ACE2(红色),DAPI(蓝色);D. 肺感染细胞的免疫荧光染色分析。hACE2(白色)、CC10(红色)、β-IV-Tubulin(青色)、PDPN(品红)和SPC(金色)。
接着,为了验证感染SARS-CoV-2的hACE2小鼠是否产生了与新冠肺炎患者相似的病理特征,对感染SARS-CoV-2的小鼠的肺切片进行组织病理学检查、免疫组化(IHC)和免疫荧光染色。结果显示,与SARS-CoV-2感染的野生型小鼠比较,青年和老年hACE2小鼠均发生间质性肺炎,表现为炎症细胞浸润、肺泡间隔增厚和血管系统损伤。老年小鼠肺泡上皮细胞病变较多,局灶性出血较多(图3A)。相比WT小鼠,免疫组化染色分析显示SARS-CoV-2感染引起老年hACE2小鼠更多中性粒细胞(Neu+)和巨噬细胞(CD68+)浸润(图3B和3C)。免疫荧光染色显示SARS-CoV-2直接感染肺内CD68+巨噬细胞,导致老年hACE2小鼠C-Casp3+凋亡显著(图3D)。另外,与青年小鼠相比,细胞因子分析显示感染SARS-CoV-2后老年hACE2小鼠中产生更多的细胞因子,包括Eotaxin(嗜酸性粒细胞趋化因子),G-CSF(粒细胞集落刺激因子), IFN-g(干扰素), IL-9(白细胞介素9)和mip -1b(巨噬细胞炎症蛋白1b)(图3E)。因此可以看出,hACE2小鼠体内不仅病毒复制旺盛,而且感染SARS-CoV-2后会引起小鼠肺部病理变化。
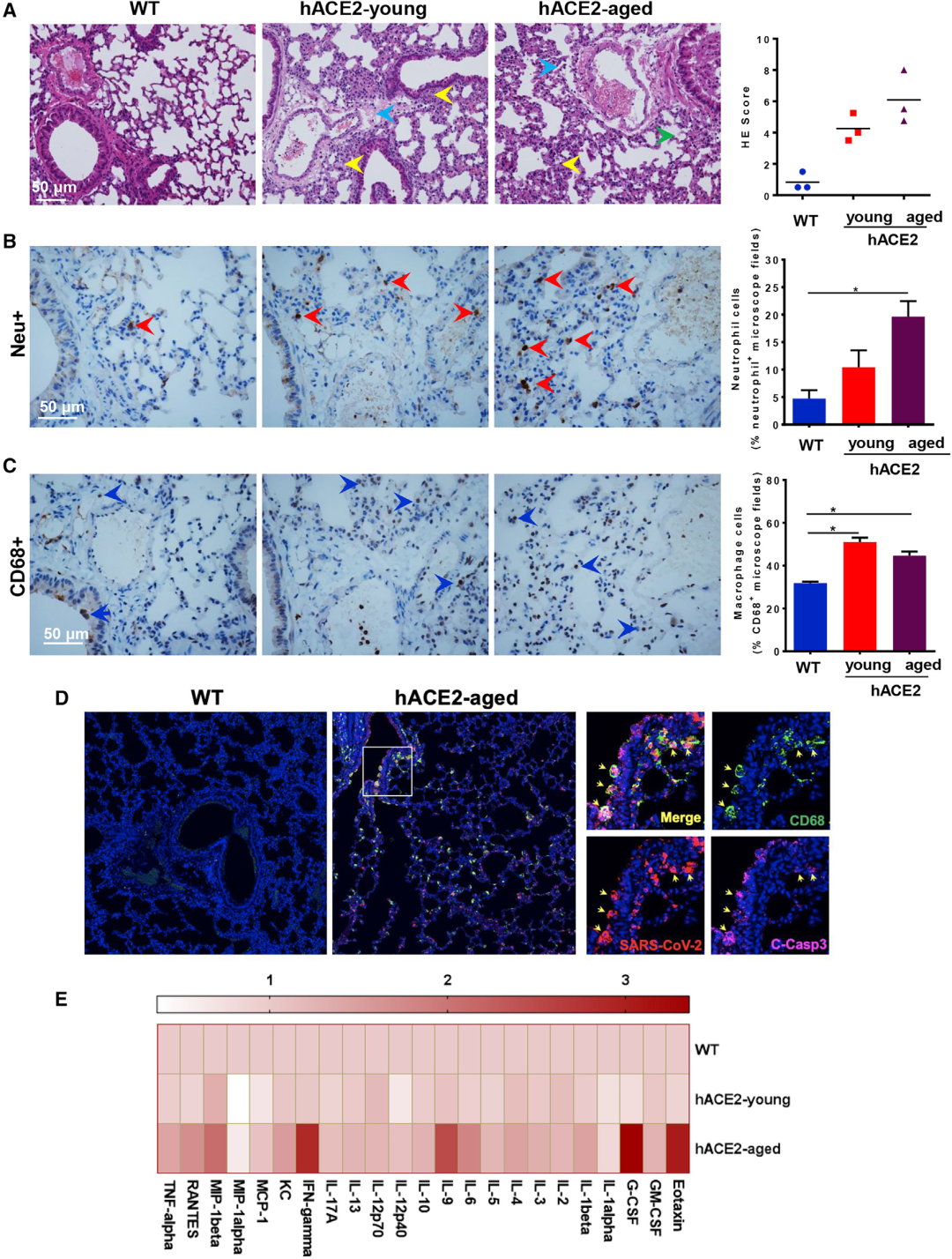
图3.A. 染色结果显示hACE2小鼠炎症细胞浸润(黄色箭头)、肺泡间隔增厚、局灶性出血(绿色箭头)和血管系统损伤(蓝色箭头);B和C. hACE2小鼠感染SARS-CoV-2后中性粒细胞(Neu+)和巨噬细胞(CD68+)免疫组化染色分析;D. 石蜡肺切片免疫荧光分析;E. 感染SARS-CoV-2后小鼠血清中细胞因子的产生
SARS-CoV-2主要通过飞沫和人的密切接触传播,但部分患者出现腹泻、腹痛、呕吐等胃肠道症状,在新冠肺炎患者的粪便中也检测到病毒RNA。基于此,研究人员通过对小鼠进行SARS-CoV-2灌胃处理,研究SARS-CoV-2是否能通过胃内途径在hACE2小鼠中建立生产性感染(图4A)。虽然接种的3只hACE2小鼠没有表现出临床症状,但有两只小鼠的气管(2.9 *106 copies/g)和肺(3.2 *106 copies/g)中检测到高水平的病毒RNA(图4B), 这与经鼻途径感染的小鼠相当。另外,在hACE2小鼠的肺气道中也检测到SARS-CoV-2 S蛋白的表达(图4C),研究人员还观察到经灌胃处理感染SARS-CoV-2的hACE2小鼠发生间质炎症,肺泡间隔增厚(图4D)。结果表明,通过对hACE2小鼠灌胃SARS-CoV-2也可以建立生产性感染,并导致小鼠的肺部病理改变。

图4.A. 用4×106 PFU的SARS-CoV-2病毒对4.5周龄WT C57BL/6小鼠和hACE2小鼠(n = 3)进行灌胃处理,并在接种第5天时杀死小鼠采集主要组织和血清;B. 组织中SARS-CoV-2病毒RNA的分布;C. 小鼠肺切片免疫荧光染色,SARS-CoV-2 S蛋白(绿色)和DAPI染色(蓝色);D. 小鼠肺切片的组织病理学分析,黄色箭头示肺泡间隔增厚。
综上,hACE2小鼠通过鼻内和胃内两种方式均可实现SARS-CoV-2的感染,在肺Clara细胞和巨噬细胞中病毒复制旺盛. 其中老年hACE2小鼠表现出的病理变化与COVID-19病人的病理变化更为接近。hACE2小鼠模型为研究SARS-CoV-2的传播和发病机制提供了一个小动物模型,并为了解人类感染SARS-CoV-2后的临床表现提供了依据,同时,这一模型对测试对抗SARS-CoV-2的疫苗和治疗方法也有价值。
原文链接:https://www.sciencedirect.com/science/article/pii/S1931312820303024
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)