
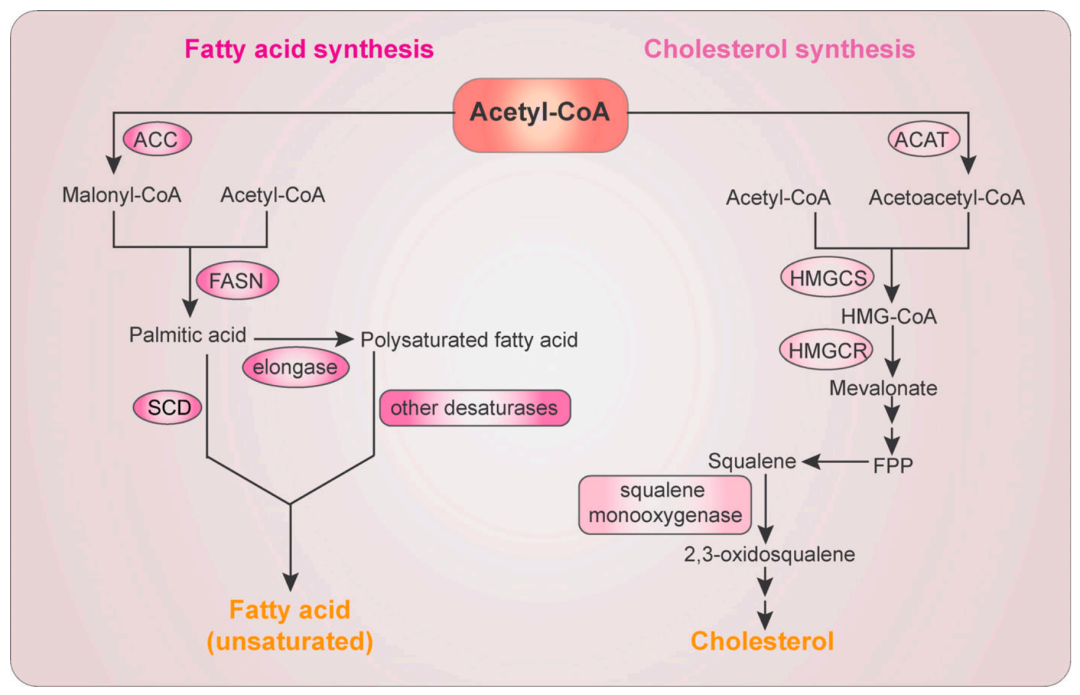
脂质是构成细胞的生物膜和结构单元的重要组成部分。此外,脂质还用于能量存储和代谢,并在多种细胞活动中起着重要的信号分子作用。脂质代谢的调控,如脂质摄取,合成和水解,对于维持细胞稳态必不可少。脂质(脂肪酸FA和胆固醇)代谢失调是癌症最突出的代谢改变之一。肿瘤微环境中营养物质的可用性不断变化,癌细胞利用脂质代谢获取癌细胞增殖、存活、侵袭、转移以及对肿瘤微环境和癌症治疗响应所需要的能量、生物膜成分和所需的信号分子(Ref:PMID33601415;IF:14+)。脂肪酸(FA)摄取:哺乳动物仅产生某些FA,其他FA,尤其是多不饱和 FA,必需从饮食中获取。质膜中已知的FA蛋白转运蛋白包括(CD36(FA转位酶)、SLC27(FA转运蛋白家族)、 FABPs(质膜FA结合蛋白)),这些基因和蛋白的表达都在癌症中上调 (Ref:PMID19185504;IF:12+)。还有研究表明CD36高表达与乳腺癌、卵巢癌、胃癌、前列腺癌的不良预后相关与口腔鳞癌转移相关(Ref:PMID27974793;IF:49+)。缺氧、肿瘤细胞中过度表达的FA转运蛋白、特异性癌基因表达和肿瘤细胞调节的基质细胞(包括脂肪细胞和成纤维细胞)可以诱导肿瘤细胞摄取细胞外FA并产生有丝分裂信号以维持肿瘤细胞增殖(Ref:PMID25263561、29398710、30837243)。脂肪酸相关往期精彩推文胆固醇摄取:肝脏是主要的胆固醇生物合成器官,胆固醇作为极低密度脂蛋白被输送到血液中,在血液中被加工成低密度脂蛋白(LDLs),再通过LDL受体(LDLRs)被外周细胞摄取。LDLRs与小细胞肺癌、乳腺癌和胰腺癌患者的不良预后呈正相关(Ref:PMID25675507;IF:12+)。正常组织中的脂肪生成主要局限于肝细胞和脂肪细胞。然而,即使存在外源性脂质来源,癌细胞也会激活脂肪生成以响应其高代谢需求 (Ref:PMID27658529;IF:60+)。脂质合成主要底物是细胞质乙酰辅酶A,由于脂肪酸和胆固醇都是由乙酰辅酶a(acetyl-CoA)通过一系列反应合成的,所以acetyl-CoA水平是产生脂质的关键因素。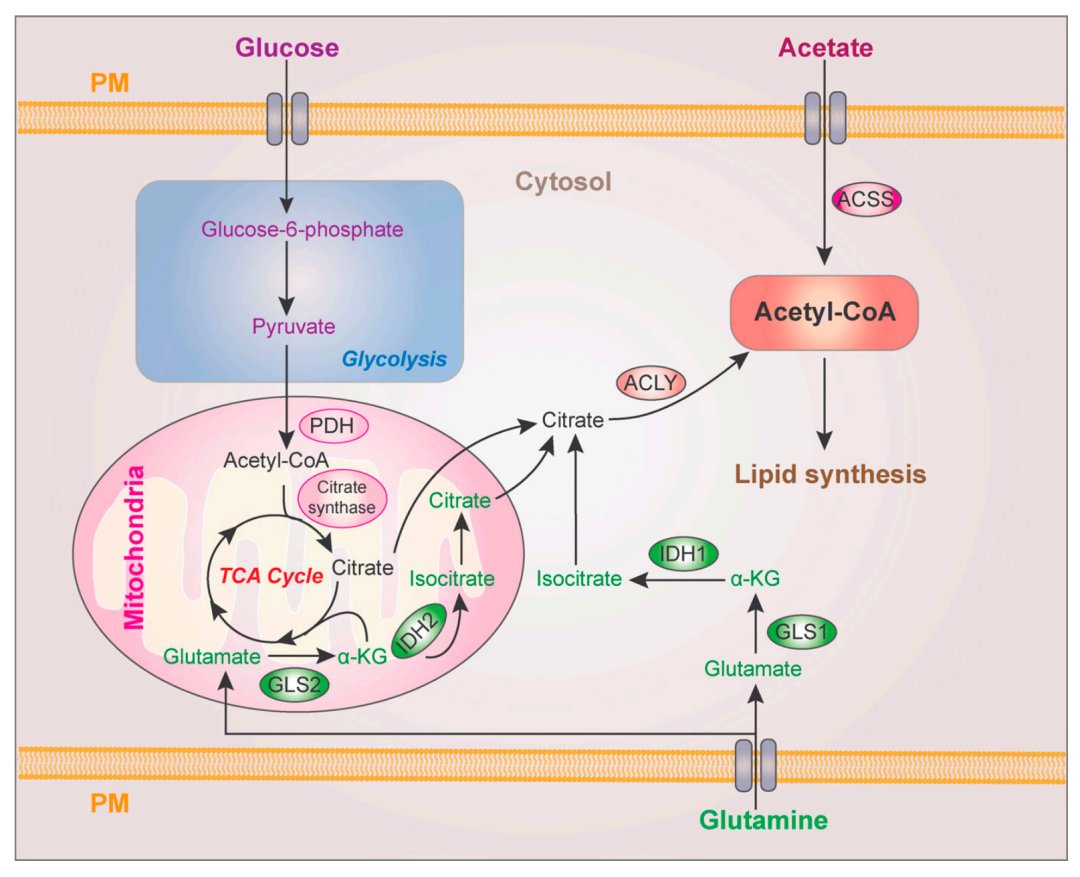
ACLY:ACLY催化柠檬酸和辅酶a转化为草酰乙酸和乙酰辅酶a,通过抑制ACLY,苯丙烯二酸降低了患者的LDL胆固醇水平。ACLY的过表达或活性增强与胶质母细胞瘤、结直肠癌、乳腺癌、肺癌和肝细胞癌的肿瘤进展相关。在各种类型的癌症中,ACLY表达的减少会降低肿瘤细胞的生存能力,抑制肿瘤细胞的增殖、侵袭和转移(Ref:PMID31858156;IF:4.6+)ACSS2:ACSS通过醋酸盐与CoA的连接产生acetyl-CoA。ACSS2被SREBP转录上调,在很大比例的肿瘤中表达,尤其是在代谢压力下对醋酸催化维持癌细胞生长至关重要(Ref:PMID25525877;IF:41+)。此外,与转录因子EB复合物中,ACSS2通过利用组蛋白去乙酰化释放的醋酸盐在基因的启动子区域局部产生乙酰辅酶A,激活溶酶体和自噬体相关基因,从而导致溶酶体生物发生和自噬,细胞存活和脑肿瘤生长(Ref:PMID28820290;IF:16+)。乙酰辅酶A羧化酶 (ACC):是脂肪酸(FA)合成的限速酶,催化acetyl-CoAacetyl-CoA羧化为丙二酰辅酶A。ACC有两种组织特异性异构体:ACC1(由ACACA编码)和 ACC2(由ACACB编码)。ACC1 是一种胞质酶,肝脏和脂肪组织中表达,对 FA 合成至关重要。ACC2则控制着线粒体对FA和FAO的摄取。ACC1在多种人类癌症中高度表达,包括乳腺癌、前列腺癌、肝癌和胃癌,ACC1 耗竭减少FA合成并诱导前列腺和乳腺肿瘤细胞的凋亡,而不是非恶性细胞的凋亡(Ref:PMID17157792;IF:31+)。ACC2高表达则与喉癌5年生存率低相关(Ref:PMID27635760;IF:17+)。FASN:FASN可以将1个acetyl-CoA和 7个丙二酰辅酶A分子缩合成16碳棕榈酸酯。FASN 过度表达和活跃通常发生在许多上皮癌及其癌前病变中,并且与癌症复发和死亡高风险相关(Ref:PMID17882277;IF:60+);FASN抑制会降低FA合成并诱导丙二酰辅酶A积累以抑制CPT1 介导的FAO,并导致随后的细胞周期停滞和肿瘤细胞凋亡(Ref:PMID16740734;IF:12+)硬脂酰辅酶A去饱和酶 (SCD):SCD是ER中的一种限速酶,可催化硬脂酸和棕榈酸生成单不饱和脂肪酸油酸和棕榈油酸。SCD需要NADPH和氧气才能发挥作用,这也解释了为什么在缺氧条件下,癌细胞更多地依赖外源供应的不饱和FA。当细胞被剥夺外源性脂质时,随后SCD1抑制会诱导铁死亡和细胞凋亡(Ref:PMID249859404;IF:12+)。抑制SCD1能迫使肝肿瘤起始细胞通过ER应激诱导的未折叠蛋白反应分化,从而提高对索拉非尼的敏感性(Ref:PMID28647567;IF:25+)哺乳动物3-羟基-3-甲基戊二酰 (HMG)–CoA还原酶 (HMGCR):是胆固醇生物合成甲羟戊酸途径的限速酶,是一种定位于ER的糖蛋白,可将HMG-CoA 转化为甲羟戊酸。HMGCR 表达在胃癌、胶质母细胞瘤和前列腺癌中上调。HMGCR 的过表达促进了癌细胞的生长和迁移,而HMGCR敲低抑制了肿瘤发生。HMGCR 抑制剂已经靶向用于治疗具有耐药性的实体癌和血癌(Ref:PMID29899021;IF:25+)角鲨烯单加氧酶(SM,由SQLE):是HMGCR下游的第二种限速 ER 相关胆固醇生物合成酶,SQLE 基因在多种癌症中发现有拷贝数扩增,并且在非酒精性脂肪性肝病诱导肝细胞癌 中检测到过表达,并与胰腺癌的放射抗性以及乳腺癌、前列腺癌、结直肠癌和肺鳞癌的进展或预后不良有关(Ref:PMID29899021;IF:17+).脂肪生成受SREBPs家族转录调控(SREBP1a和SREBP1c (SREBF1编码)、SREBP2 (SREBF2基因编码)) 。SREBP-1c 普遍表达,而 SREBP-1a 在肠上皮、心脏和巨噬细胞中表达,而SREBP2 在肝脏和脂肪组织中表达。SREBP1主要调节FA合成基因和LDLR的表达,而SREBP2优先控制胆固醇生物合成基因的表达。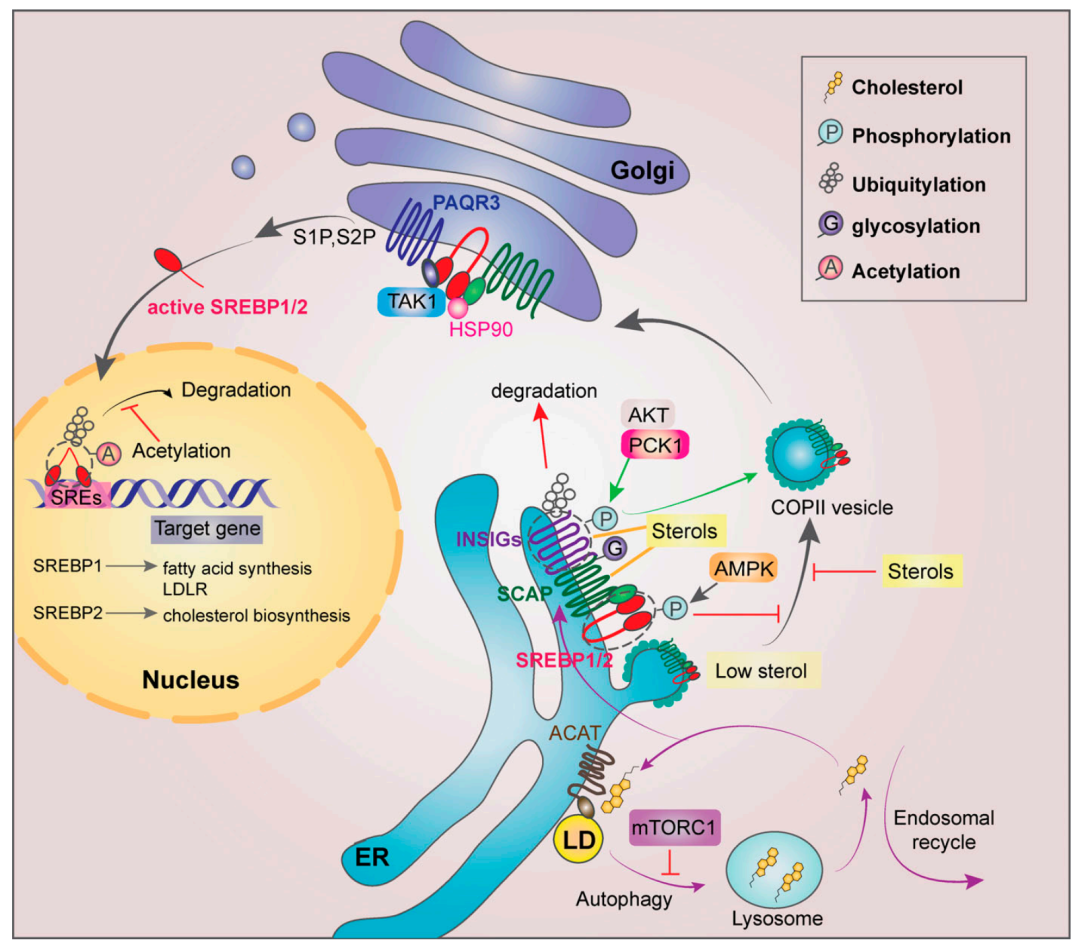
内质网中SREBP的调节:SREBP激活受ER中固醇波动调节。胆固醇与SREBP裂解激活蛋白(SCAP)结合,从而破坏SCAP 和COPII之间的相互作用,并将SREBP保留在ER中。抑制胆固醇酰基转移酶(ACAT )会积累 ER胆固醇,减少脂滴形成,并通过阻断 SREBP1 调节的基因表达来抑制胶质母细胞瘤的生长和前列腺癌细胞的侵袭性(Ref:PMID27281560;IF:17+); INSIG/SCAP/SREBP 复合物也可以以不依赖脂质的方式进行调节:磷酸化的INSIGs减少了它们与氧固醇的结合,从而激活了SREBP依赖性脂肪生成以形成肝肿瘤。此外,PCK1 介导的 INSIG 磷酸化与较差的 HCC 预后相关(Ref:PMID32322062;IF:17+)。高尔基体中SREBPs的调节:热休克蛋白90 (HSP90) 结合并稳定ER和高尔基体中的 SREBP-SCAP复合物并促进其向高尔基体的转运。高尔基体锚定蛋白孕激素和adipoQ受体3 (PAQR3) 在胆固醇消耗条件下被转录诱导,与SCAP和SREBP相互作用并将它们束缚在高尔基体上以增强 SREBP 加工并增强脂质合成 。细胞核中SREBP的调控:mTORC1 通过LPIN1的磷酸化和细胞质滞留促进成熟 SREBP1 的核定位。赖于GSK3介导的SREBP磷酸化的SCFBXW7泛素连接酶可降解核SREBP。这种磷酸化被PRMT5的 SREBP1a R321 二甲基化抑制,导致脂肪生成增加、肿瘤细胞增殖加速和HCC患者预后不良(Ref:PMID26759235;IF:12+)。SREBPs的转录调控和LXRs在脂质稳态中的作用:LXRα和LXRβ与retinoid X receptor受体形成异二聚体,并在不同的核氧固醇存在下与SREBF1启动子中的保守LXR反应元件结合,作为LXR配体,以促进脂质合成。LXR已被证明对不同肿瘤细胞的生长和存活发挥正向或负向调节作用(Ref:PMID26120082;IF:12+)脂肪酸氧化(FAO)允许长链 FA 在线粒体转化为acetyl-CoA,进入 TCA 循环,生成ATP和苹果酸酶依赖性NADPH。多类癌症,例如具有K-Ras突变的肺癌、三阴性乳腺癌和神经胶质瘤,都表现出较高的 FAO 活性,FAO通路蛋白过表达(Ref:PMID23446547;IF:60+)。过度活跃的FAO可能具有细胞毒性。在胶质母细胞瘤细胞中,抑制DGAT1会导致过量的FAO和ROS 产生和细胞凋亡(Ref:PMID32559414;IF:27+)。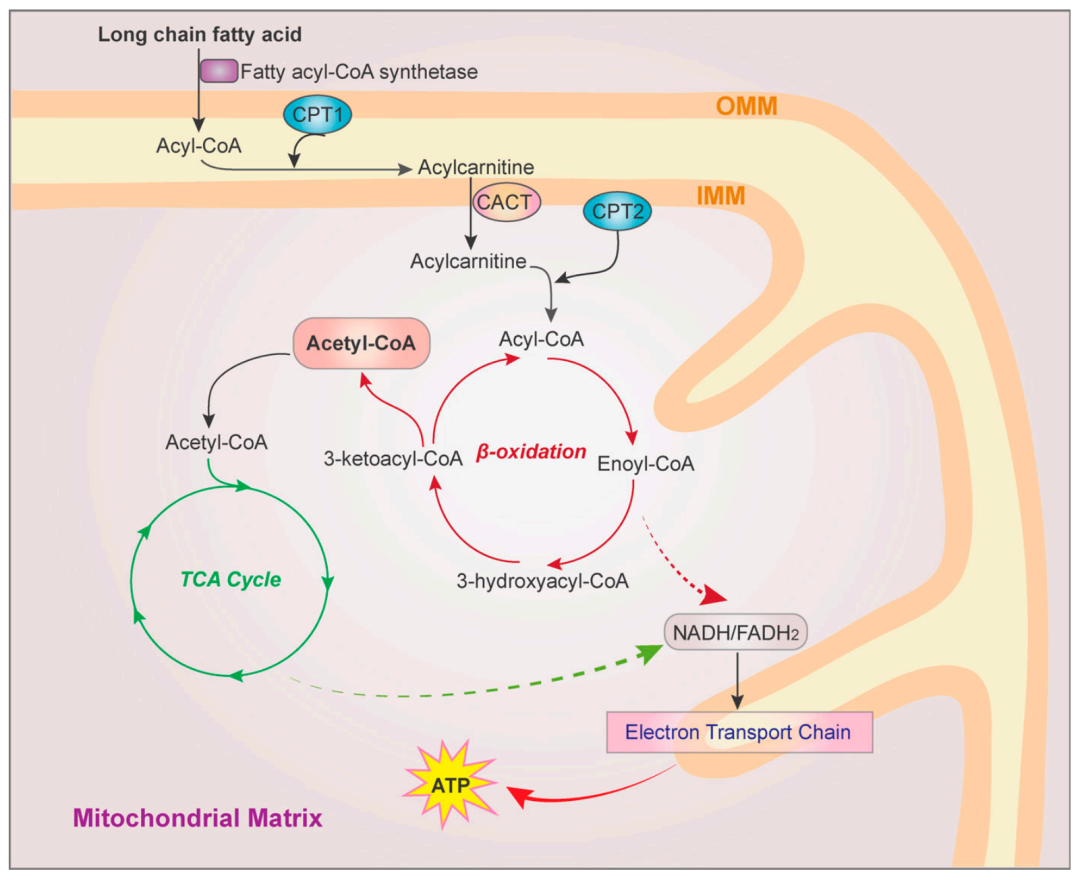
致癌信号与脂质代谢之间的整合和相互调节促进了癌细胞的生长、存活、增殖、迁移、侵袭和转移。癌细胞和肿瘤微环境中其他细胞(e.g.免疫细胞、脂肪细胞、内皮细胞和成纤维细胞)中的脂质代谢是动态调节和相互关联的。开发在不同水平上干预脂质代谢的癌症治疗药物成为新的挑战。靶向胆固醇合成,他汀类药物,如 HMGCR抑制剂,在多项临床试验中作为抗癌剂进行测试(Ref:PMID27562463;IF:60+);靶向FA合成,FASN抑制剂 TVB-2640 目前正在 II 期临床试验中。癌细胞中的脂质代谢不仅可以通过细胞内致癌信号进行调节,还可以通过由各种细胞、细胞因子、生长因子、DNA、RNA和包括脂质在内的营养物质组成的肿瘤微环境来调节。反过来,异常的脂质代谢会改变癌细胞中的致癌信号通路,并通过包括脂质在内的分泌成分影响邻近的正常细胞群。这种复杂性说明不仅需要研究癌细胞中的脂质代谢网络,还需要研究TME中相互作的通路以及干扰TME中细胞脂质代谢对肿瘤进展和治疗反应的影响,尤其是抗肿瘤免疫和抗血管生成反应。深入探索脂质代谢的肿瘤特异性调控能帮助发现癌症消除治疗机会。接下来我们简单介绍下近年来脂肪代谢的一些有意思的高分文章
这篇综述讨论了铁死亡期间脂质代谢发生改变,它们的相互作用调节了癌症的发生、发展、转移、治疗抵抗以及肿瘤免疫,并强调了这种相互作用在癌症中的重要性。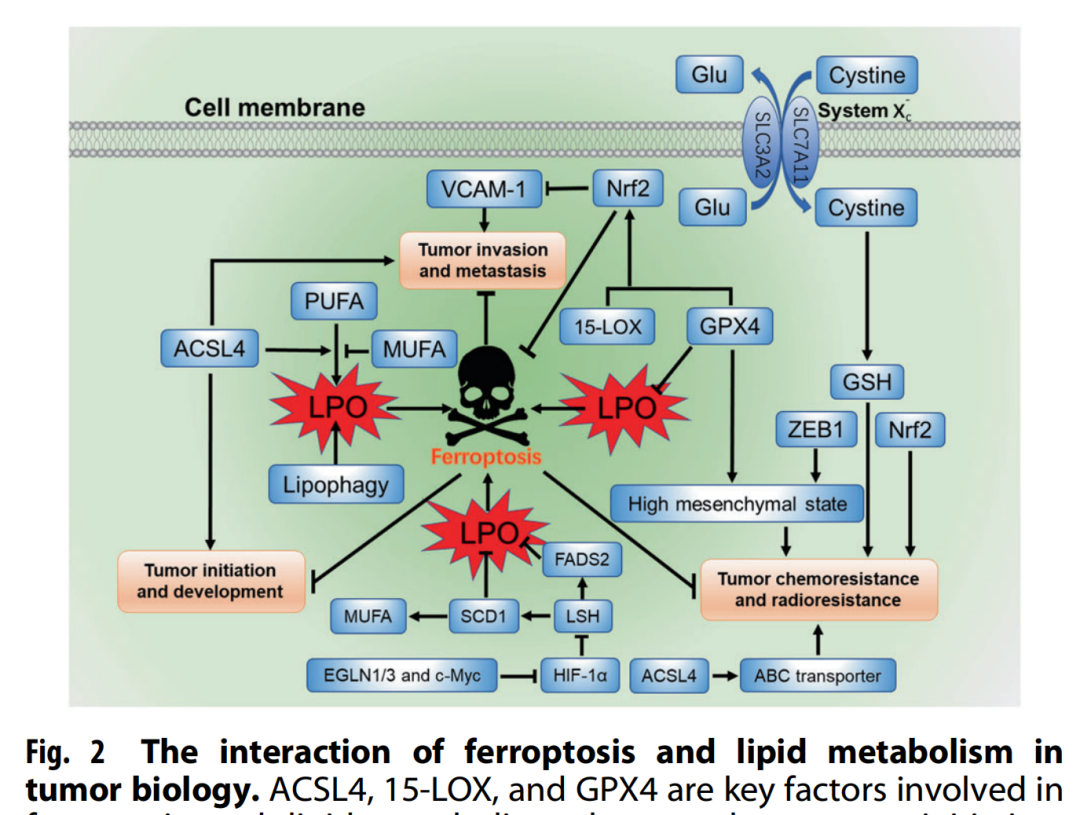
第二篇:吕志民团队联合洪明奇团队在Nature杂志上揭示了肿瘤细胞特异性脂质合成代谢机制研究
该研究的重要性主要体现在:(1) 阐明了肿瘤细胞脂质感应异常及脂质合成持续激活的重要机制;(2) 首次发现了糖异生代谢酶PCK1具有蛋白激酶活性;(3)揭示了PCK1以GTP作为磷酸基供体对蛋白底物进行磷酸化,这有别于普遍的以ATP作为磷酸基供体的蛋白激酶;(4)论述了PCK1的内质网易位是肿瘤细胞协同调节糖异生降低和脂质合成激活的重要分子机制。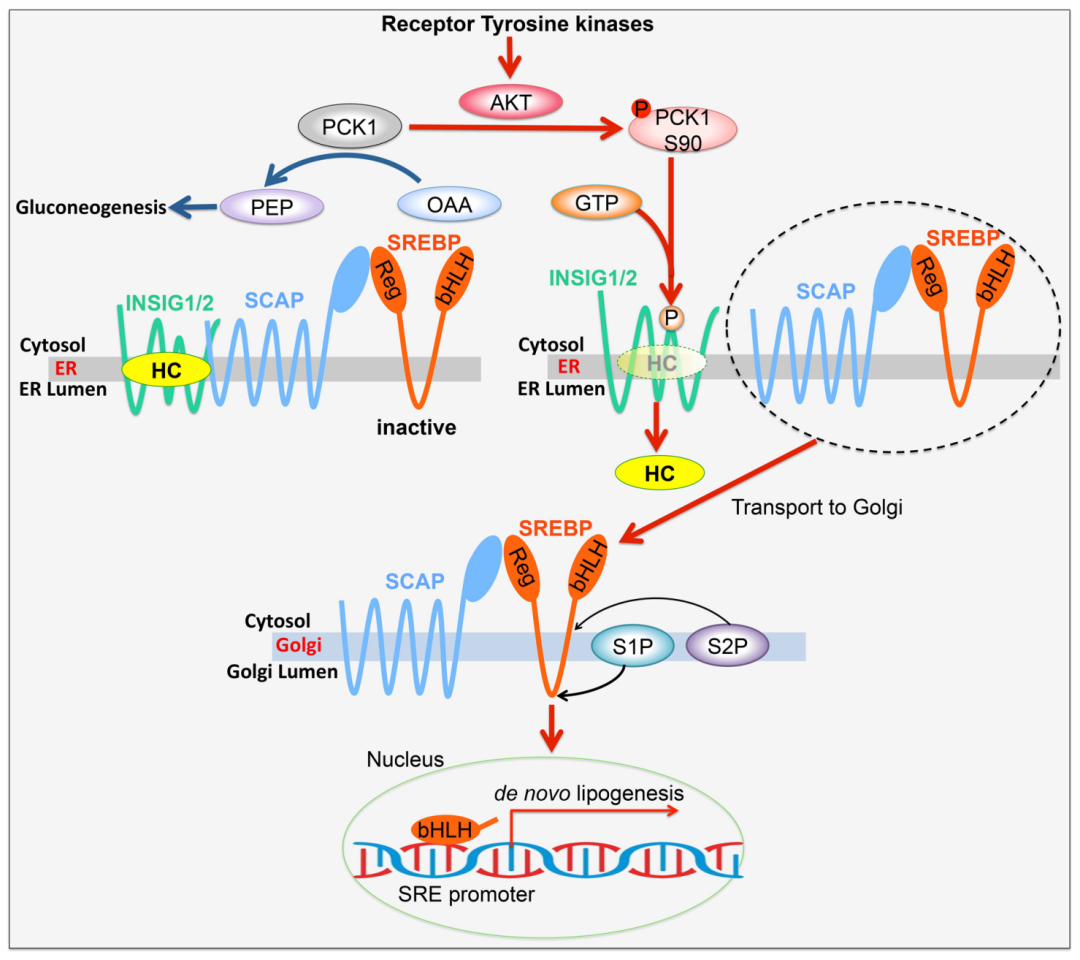
第三篇:迟洪波教授团队于《Nature》上发表阐述了脂质代谢重编程增强了肿瘤中Treg细胞的功能专一性研究
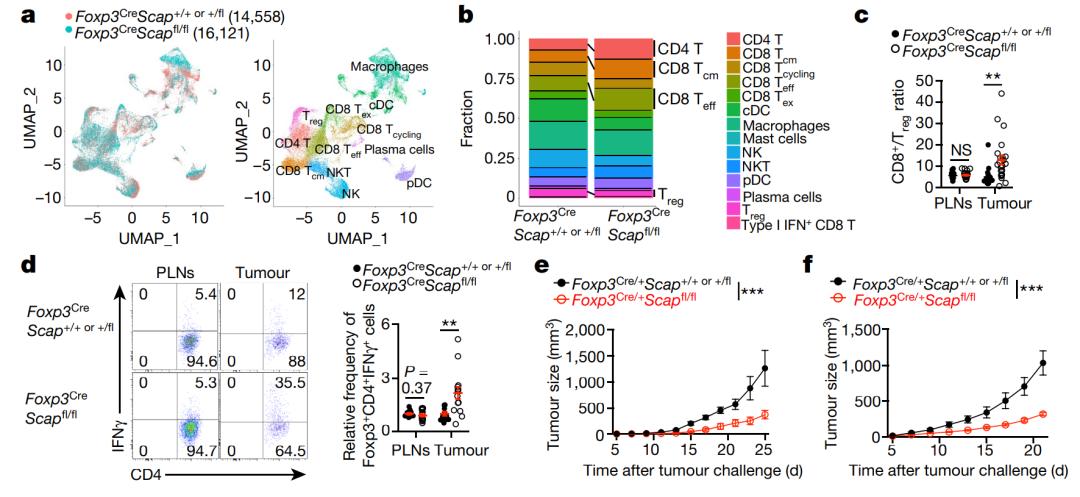
第四篇:彭光勇教授团队在 Science 子刊 Science Translational Medicine 期刊发表了肿瘤微环境中T细胞衰老与脂质代谢调控之间的联系,表明靶向脂质代谢可以进一步提高癌症免疫疗法效果,也为肿瘤免疫疗法提供了新的靶点的研究论文
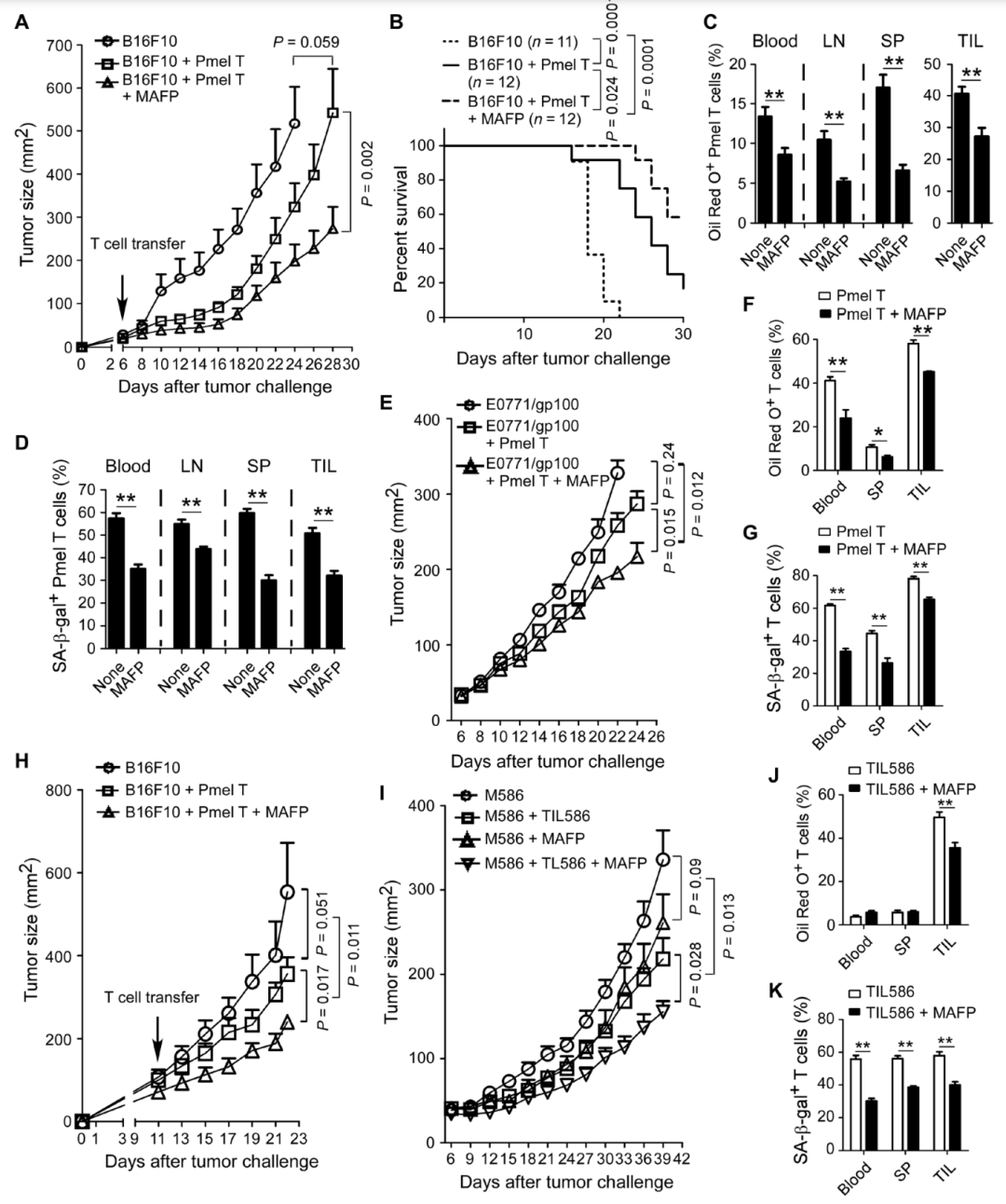
涉及肿瘤能量代谢的都是潜在的研究热点。经过对癌症中脂质代谢长篇大论的絮叨后,相信大家应该对癌症脂质代谢有了全面的了解,我们继续对全网现有的脂质代谢纯生信文章进行了地毯式搜索,发现了两篇做脂质代谢预后signature的文章,我们也设计了脂质代谢的个性化思路,感兴趣扫码。
第一篇:肾透明细胞癌脂代谢预后signature(IF:6+)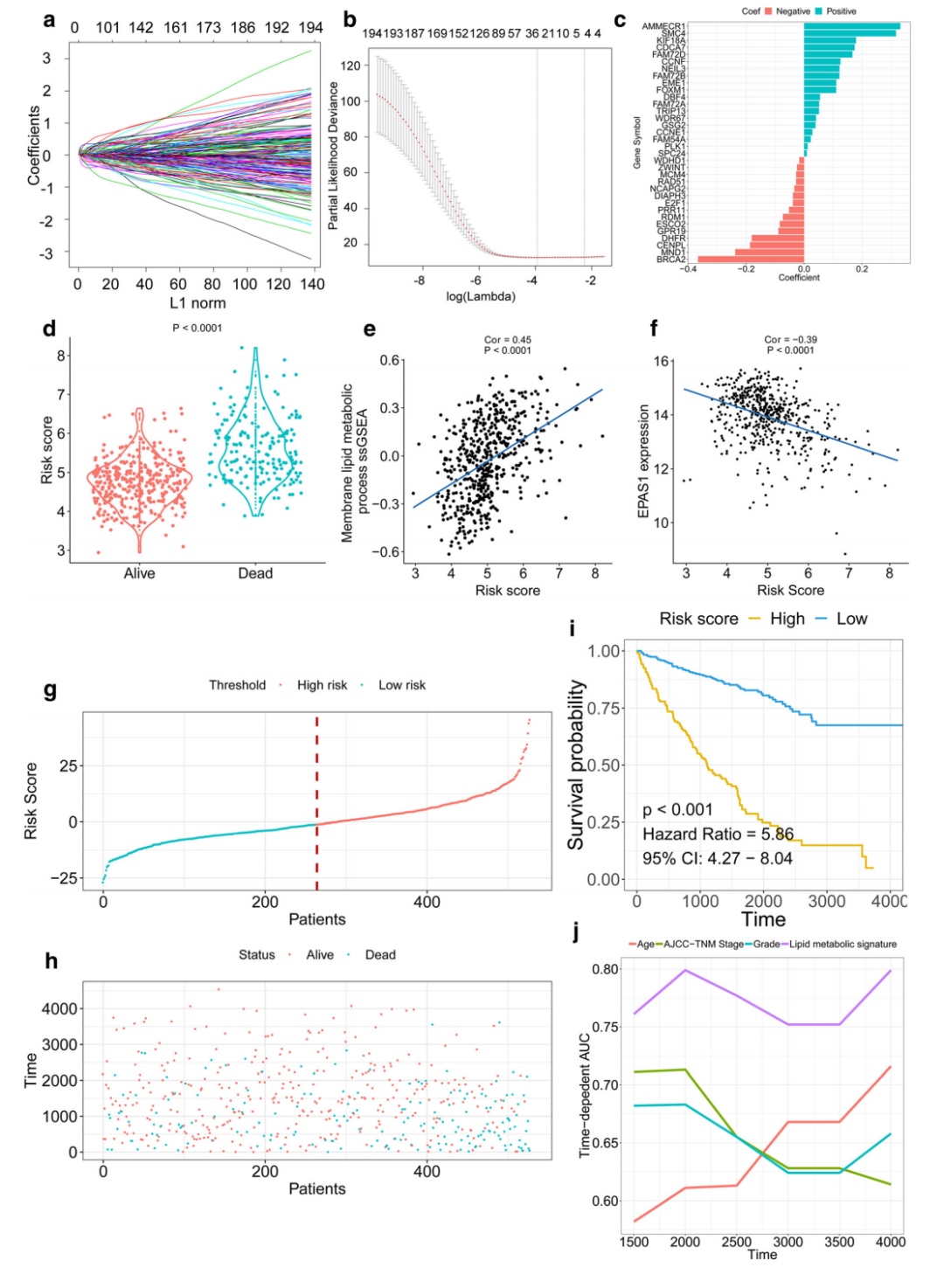
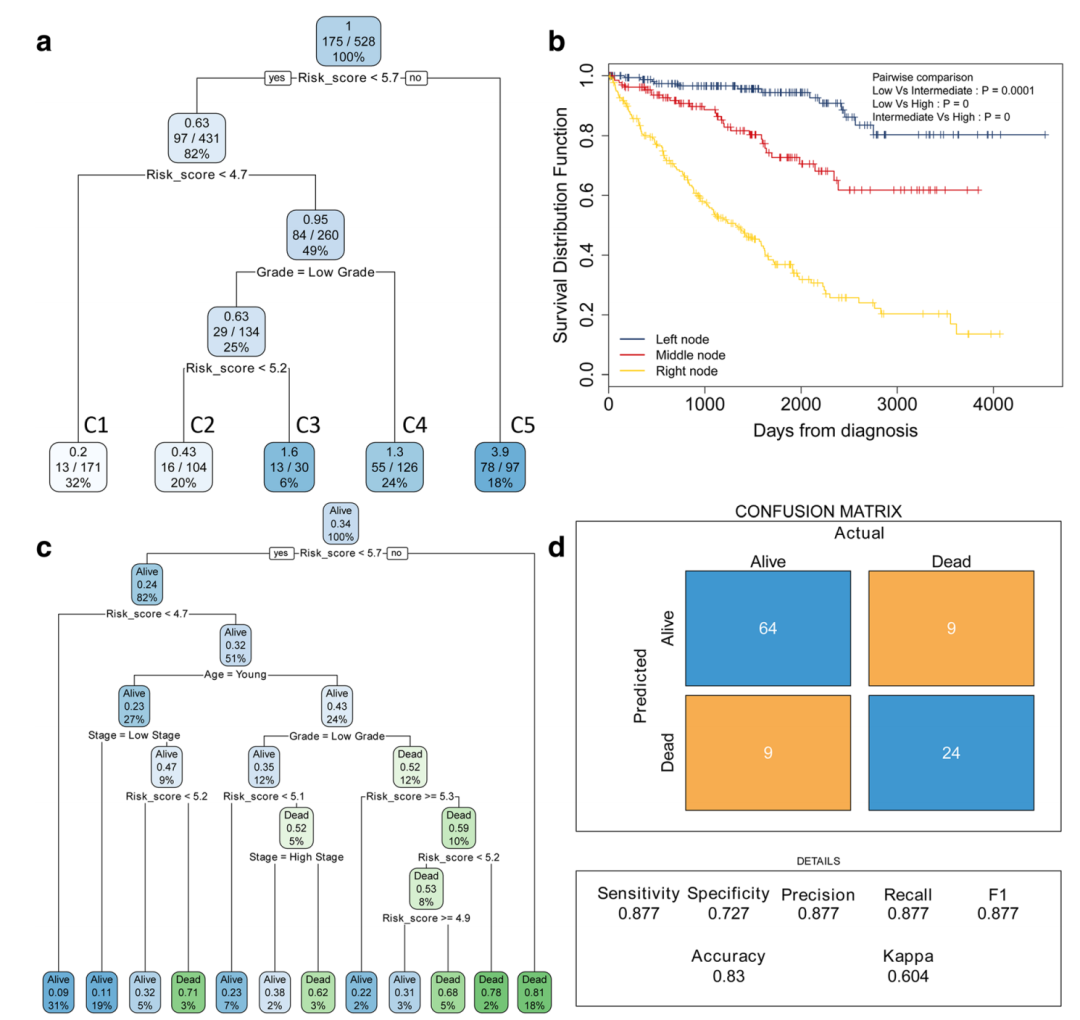
第二篇:肝癌免疫相关的脂代谢和预后signature篇(IF:4+)

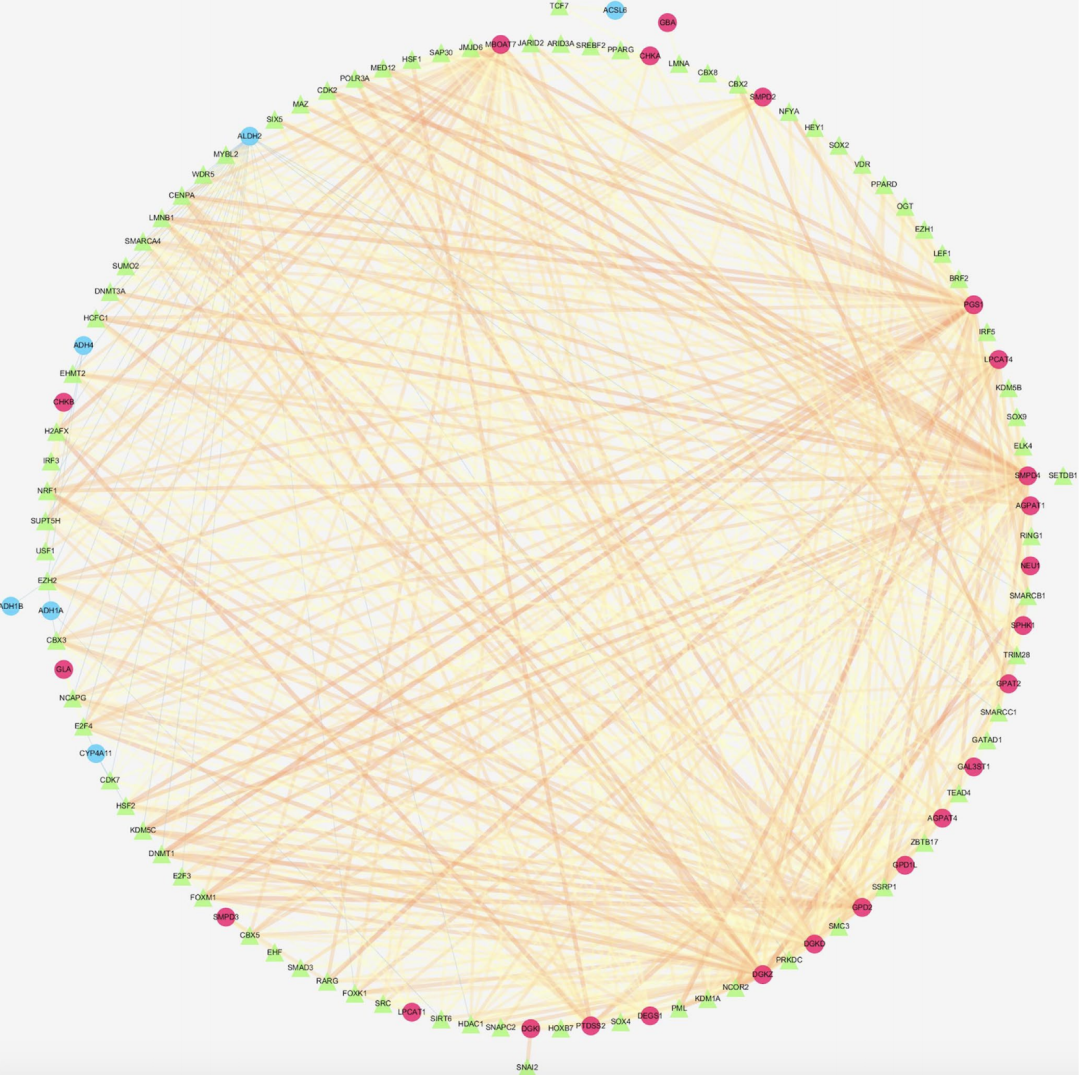
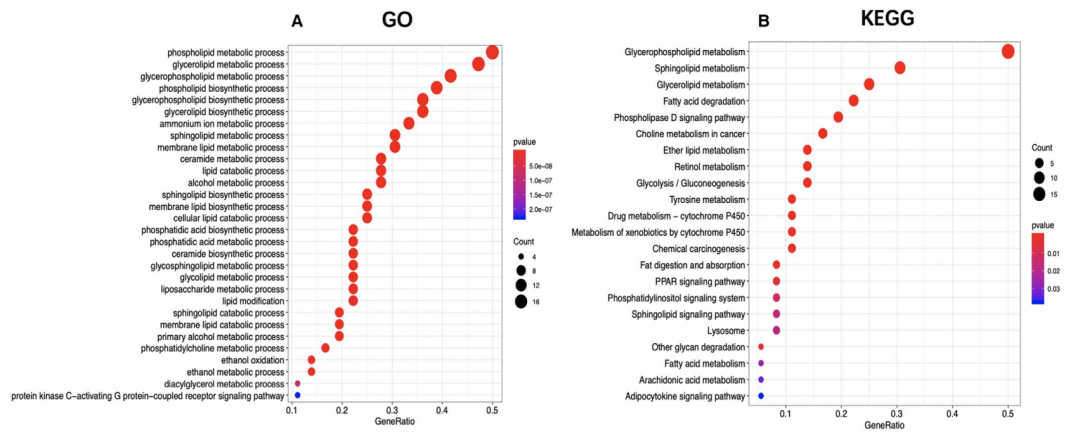
脂代谢因子表达失调、转录因子调控网络构建(这个网络图不怎么好看呀)、富集分析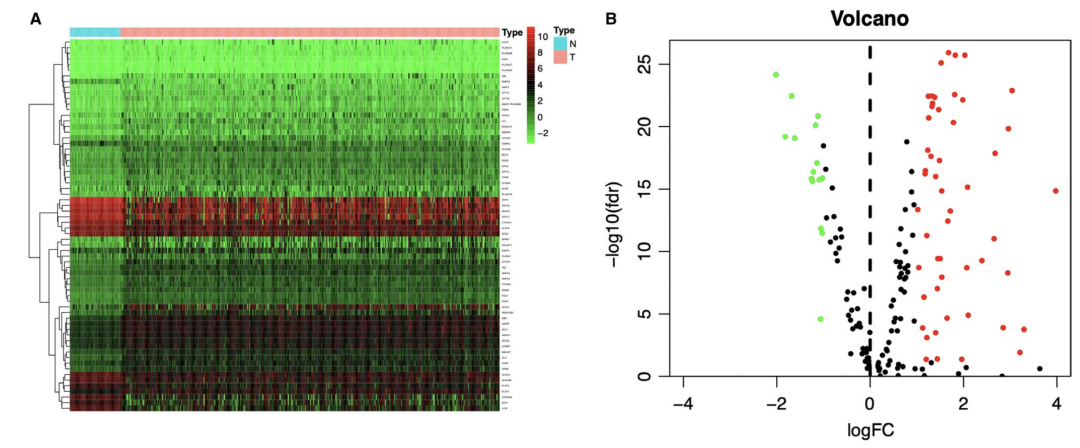
筛选预后脂代谢基因构建预后signature分析预测效能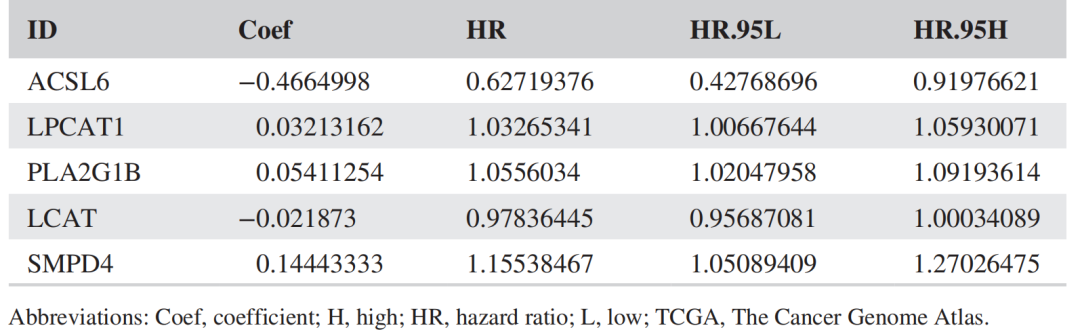
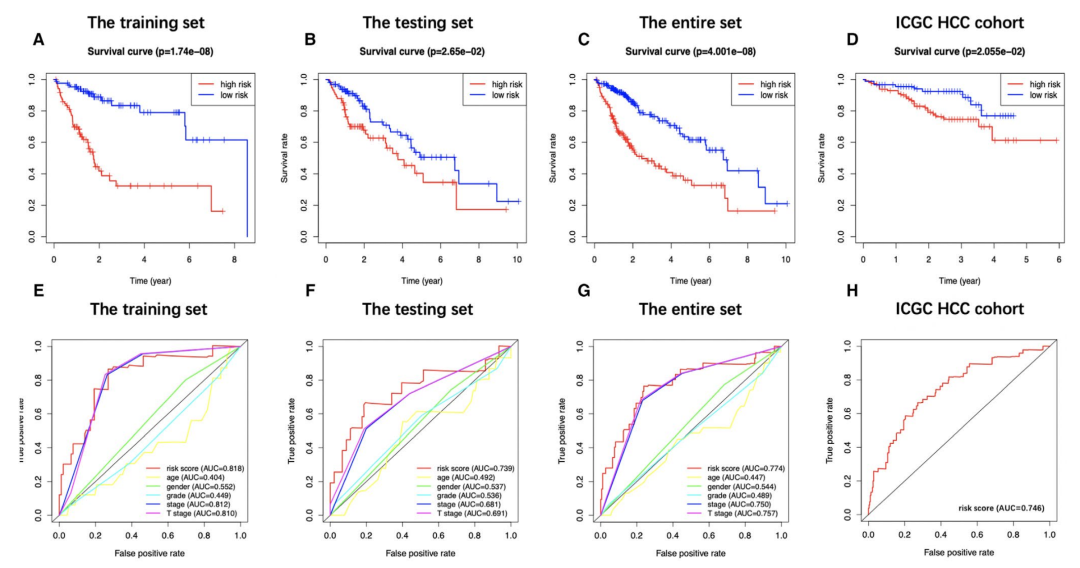
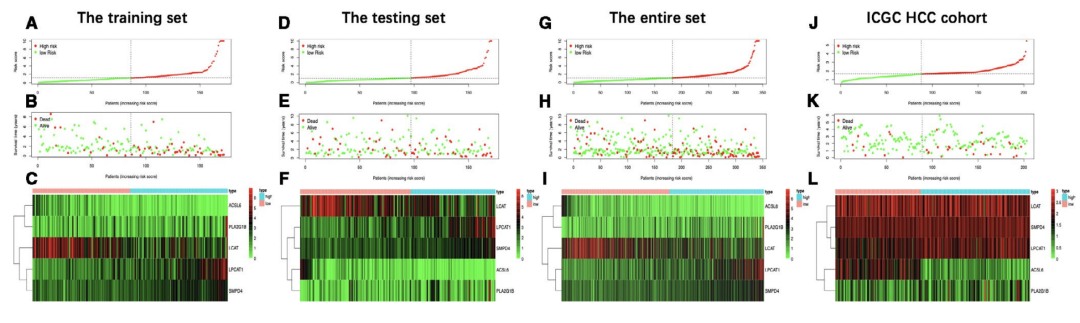
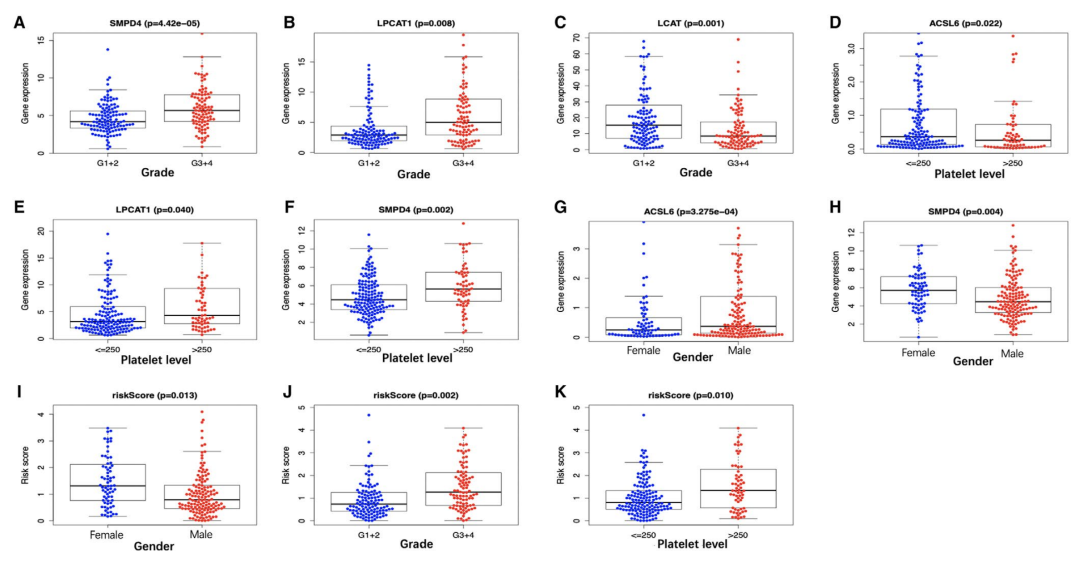
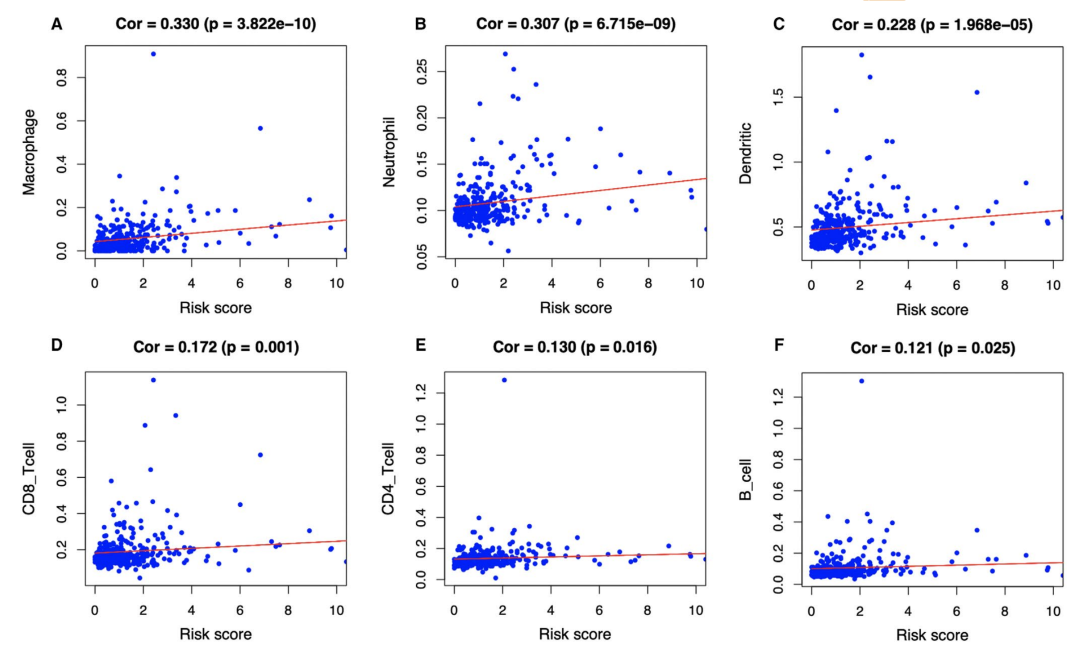
结合预后signature的免疫基因集的富集分析
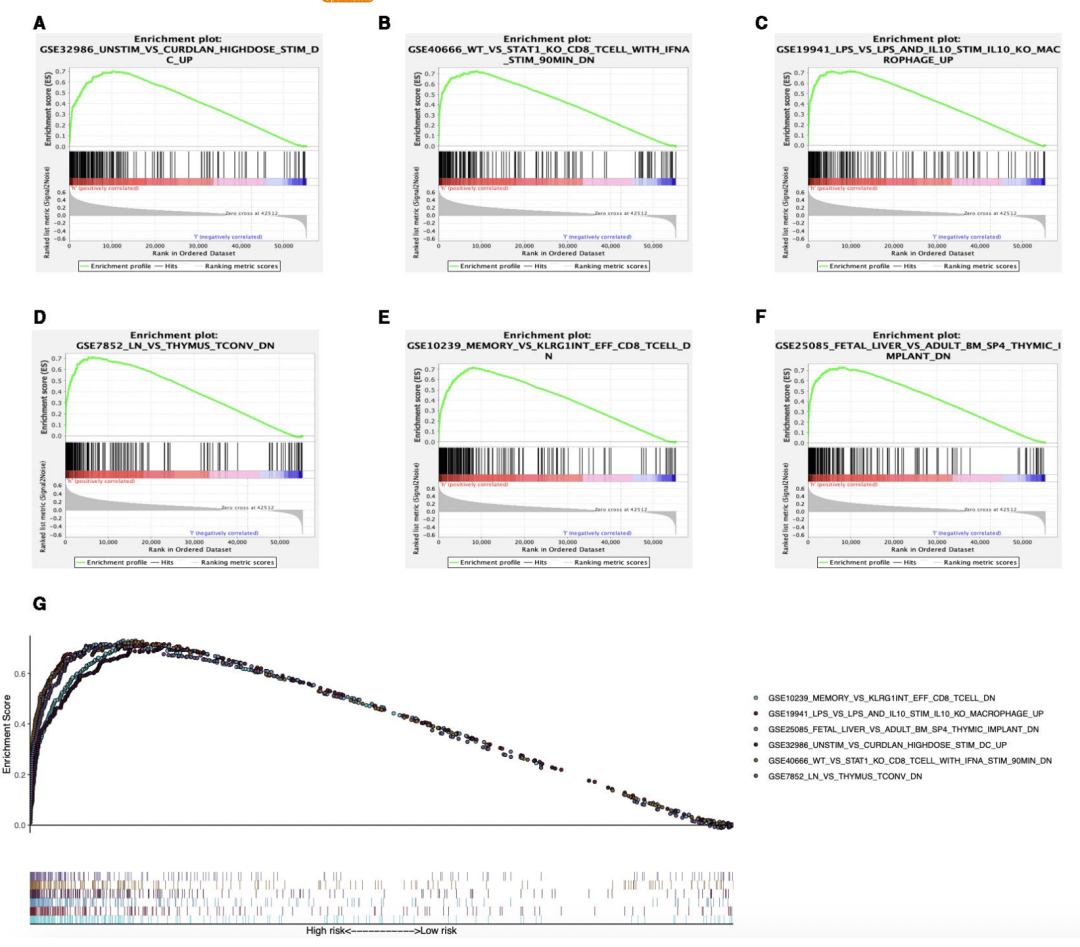
简简单单几张图就完成了脂质代谢的纯生信分析,这两个文章都有一个共同的主旨,不管什么样的方式,都是在构建一个能够对癌症预后分层的预后signature,那么除了这种形式的预后分析还有其它的吗,生信人为你准备了一系列的癌症个性化脂代谢思路。
1、Lipid metabolism and cancer2、The gluconeogenic enzyme PCK1 phosphorylates INSIG1/2 for lipogenesis3、Lipid signalling enforces functional specialization of T reg cells in tumours4、Reprogramming lipid metabolism prevents effector T cell senescence and enhances tumor immunotherapy
百度浏览
来源 : 生信人
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





























发表评论
注册或登后即可发表评论
登录注册
全部评论(0)