2023-11-03 来源 : 药论
加利福尼亚州和中国上海,2023 年 10 月 27 日(环球通讯社)-- Coherus BioSciences, Inc.和上海君实生物科技股份有限公司今天宣布,美国FDA批准LOQTORZI™(特瑞普利单抗-tpzi)与顺铂和吉西他滨联合用于一线治疗成人转移性或复发性局部晚期鼻咽癌,以及作为单一疗法,用于治疗在含铂化疗期间或之后疾病进展的复发性、不可切除或转移性鼻咽癌成人患者。
此次批准是基于 JUPITER-02 3 期研究和 POLARIS-02 2 期研究的结果,与患者的 PD-L1 状态无关。LOQTORZI 是一种下一代程序性死亡受体-1 (PD-1) 单克隆抗体,可在 PD-1 受体的独特位点高效阻断 PD-1 配体 PD-L1 和 PD-L2,从而增强免疫系统的功能激活并杀死肿瘤,特瑞普利单抗是首个FDA批准用以治疗鼻咽癌的药物。

参考1
早在2023年5月中下旬,美国FDA完成了对特瑞普利单抗的生产现场核查。到9月下旬,合作方Coherus表示,FDA已完成对中国三个临床中心的临床研究现场检查,这些临床中心招募了两项关键临床试验的受试者,支持特瑞普利单抗BLA用于一线治疗转移性或复发性鼻咽癌(NPC)或作为二线或以上一线治疗。
在 JUPITER-02 3 期研究中,LOQTORZI 联合化疗显着改善了无进展生存期 (PFS),与单独化疗相比,疾病进展或死亡风险降低了 48%。LOQTORZI 还证明了总体生存率 (OS) 具有统计学意义和临床意义的改善,与单独化疗相比,治疗可使死亡风险降低 37%。在 POLARIS-02 临床研究中,LOQTORZI 在既往化疗失败的复发性或转移性鼻咽癌患者中表现出持久的抗肿瘤活性,客观缓解率 (ORR) 为 20.5%,疾病控制率 (DCR) 为 40.0%,中位缓解率OS 为 17.4 个月,安全性可接受。
特瑞普利单抗结合独特表位,具有高亲和力。
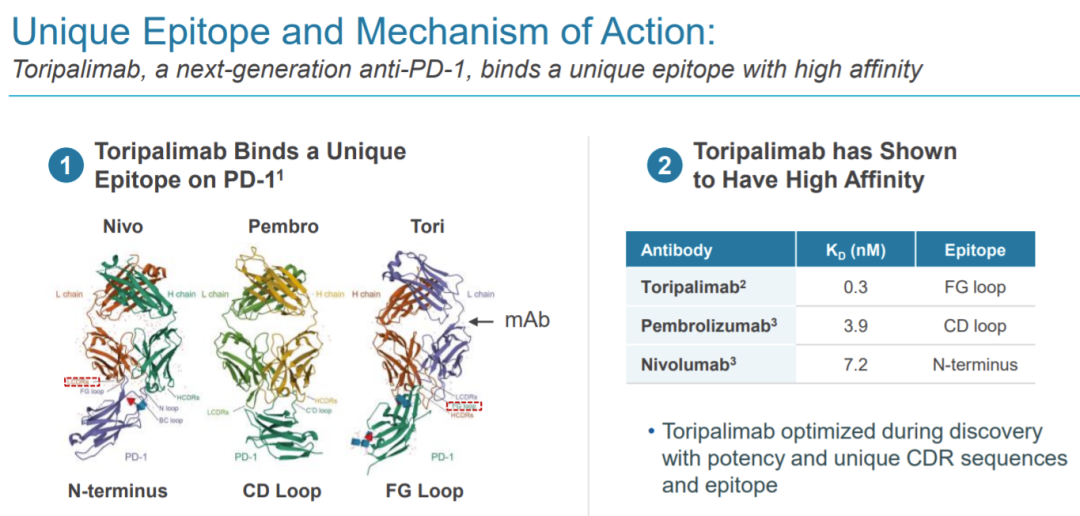
一线治疗鼻咽癌的三期临床中,特瑞普利单抗+化疗相比于化疗的mPFS分别伟11.7个月 vs 8.0个月,ORR为77% vs 66%。
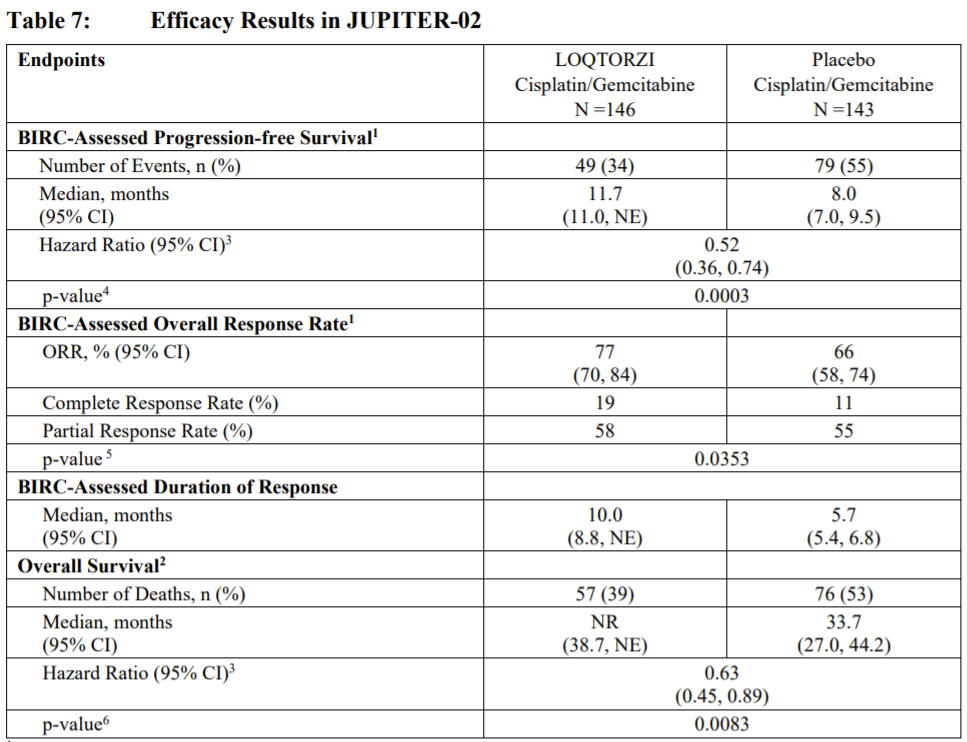
生存曲线数据如下。

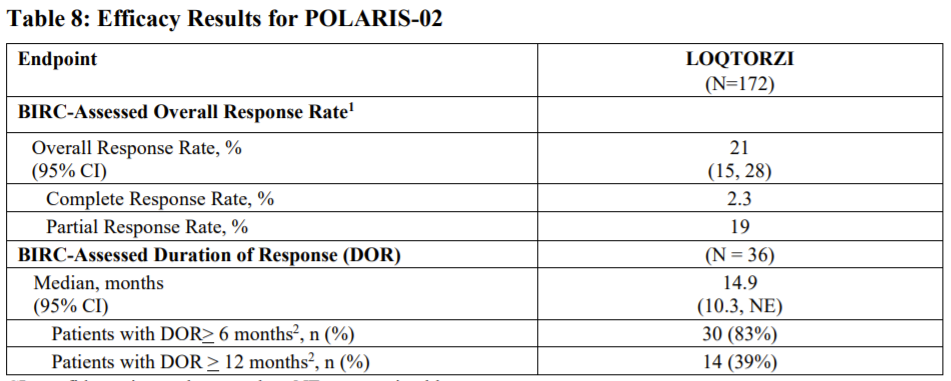
对于经治疗的鼻咽癌,Loqtorzi治疗的ORR为21%,mDoR为14.9个月。
特瑞普利单抗注射液是我国批准上市的首个国产以PD-1为靶点的单抗药物,获得国家科技重大专项项目支持,ZL201310258289.2《抗 PD-1 抗体及其应用》获第二十二届“中国专利金奖”。
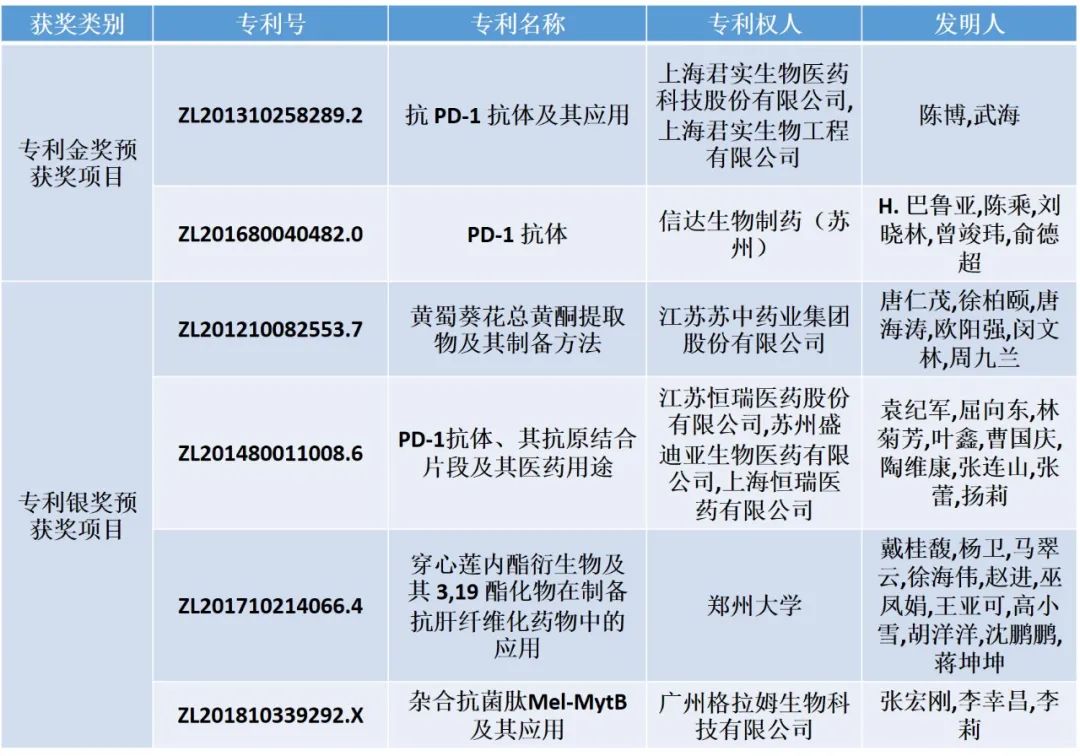
第二十二届中国专利金银奖获奖名单(生物医药)
特瑞普利单抗至今已在全球(包括中国、美国、东南亚及欧洲等地)开展了覆盖超过15个适应症的40多项由公司发起的临床研究。正在进行或已完成的关键注册临床研究在多个瘤种范围内评估特瑞普利单抗的安全性及疗效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、肾癌及皮肤癌等。
截至目前,特瑞普利单抗已在中国获批6项适应症:用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗(2018年12月);用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗(2021年2月);用于含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌的治疗(2021年4月);联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗(2021年11月);联合紫杉醇和顺铂用于不可切除局部晚期/复发或远处转移性食管鳞癌患者的一线治疗(2022年5月);联合培美曲塞和铂类用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌的一线治疗(2022年9月)。
值得一提的是,2022年12月和2023年2月,欧洲药品管理局(EMA)和英国药品和保健品管理局(MHRA)分别受理了特瑞普利单抗联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗以及联合紫杉醇和顺铂用于不可切除局部晚期/复发或转移性食管鳞癌患者的一线治疗的上市许可申请(MAA)。

PD-1/PD-L1免疫检查点抑制剂的作用原理是这样的,肿瘤细胞上调PD-L1表达,后者与T细胞表面的PD-1结合,PD-1和PD-L1结合启动T细胞的程序性死亡,肿瘤细胞从而实现“免疫逃逸”。PD-1或PD-L1抑制剂阻断PD-1与PD-L1结合,恢复T细胞抗肿瘤活性。一旦抗肿瘤免疫循环建立,可以产生持久的抗肿瘤效应。
鼻咽癌是一种侵袭性癌症,起病于鼻咽部,即鼻子后面和颅底附近的咽喉上部。由于原发肿瘤的位置,很少选择手术治疗,局部疾病患者主要接受放疗和化疗。
参考:
1.investors.coherus.com/news-releases/news-release-details/coherus-and-junshi-biosciences-announce-fda-approval-loqtorzitm#
2.国家知识产权局官网.
3.上市公司公告
4.Wu, Q., Jiang, L., Li, Sc. et al. Small molecule inhibitors targeting the PD-1/PD-L1 signaling pathway. Acta Pharmacol Sin 42, 1–9 (2021).
声明:本文仅是介绍医药疾病领域研究进展或简述研究概况或分享医药相关讯息,并非也不会进行治疗或诊断方案推荐,也不对相关投资构成任何建议。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)