2022-08-05 来源 : i医时空 ,作者一豆
随着药物研发的快速发展,临床上可选择的治疗手段和药物不断丰富。那么问题就来了,我们应该如何对这些“相似”药物做出最佳的治疗选择呢?本文将基于一些问题,逐步为大家揭秘在没有头对头RCT证据的情况下,如何对两种药物的有效性进行比较。
Q1
如何比较A药与B药?
来自墨尔本大学的Hansoo Kim于2013年汇总了药物疗效比较方法(见图1)。主要分为直接比较(1)-(2)和间接比较(3)-(5)。
图1-(1)头对头直接比较(H2H)
我们常见的为随机对照试验RCT,A药一组,B药一组,患者随机分配到A药或者B药,A与B比较,得出优效或者非劣效结果。该方法是比较两种药物有效性和安全性的金标准。
图1-(2)单纯直接比较(Naive direct comparison,NDC)
把A药和B药数据,直接进行比较,没有统计学假设和检验。
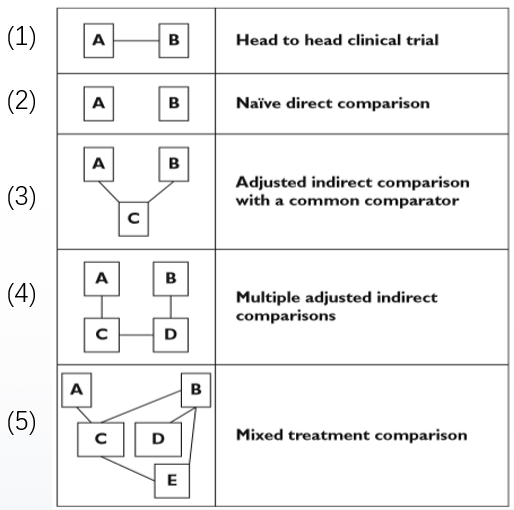
图1
基于商业角度,药厂都会避免在同类产品中做头对头的直接比较研究,除非对方已经是标准治疗,而且自认为胜算很大。在缺乏头对头直接比较(RCT)证据下的同类药物中,如何判断选择A还是B呢?
1997年,Bucher HC提出了间接比较方法(indirect comparison),间接比较的方法很多。如图1(3)-(5)。
图1-(3) 调整间接比较(Adjusted indirect comparison,AIC):
比较A药与B药,二者无直接比较的RCT证据,仅有他们分别与C药比较的RCT,C成为A,B的共同对照。于是,我们可借助C药来间接评价A与B的疗效。该方法中的匹配调整间接比较(Matching-adjusted indirect comparison,MAIC),是目前临床试验常见的间接比较方法。
图1-(4) 多重调整间接比较(Multiple adjusted indirect comparisons,MAC):
比较A药与B药,但没有共同对照组C药,可以通过两个及以上药物进行间接比较。该方法的比较关系更复杂,中间多了一个甚至更多的药物作为桥梁,不确定性大大增加。
图1-(5) 混合比较(Mixed treatment comparison MTC):
结合了方法AIC和H2H研究。应用贝叶斯方法既纳入间接比较的结果,又纳入直接比较的结果,进行更全面的分析。混合比较法MTC是目前网状meta分析(Network meta-analysis, NMA)采用的核心方法。
总结
比较A药与B药,主要有两类方法:
1) 头对头直接比较(e.g. H2H RCT);
2) 间接比较(e.g. MAIC, MTC)。
本文重点讨论间接比较方法,我们结合案例探讨目前应用最多的方法:
1)图1-(3) 调整间接比较(AIC):常见于匹配调整间接比较MAIC(本文将着重介绍此项),主要分为以下两类分析方法:
a)Anchored MAIC: 锚定匹配调整间接比较法
b)Non-Anchored MAIC: 非锚定匹配调整间接比较法
2)图1-(5) 混合比较(MTC):常见于网状meta分析NMA(下回详述)
Q2
什么类型的研究和数据,可以做匹配调整间接比较?
下表汇总了MAIC常见的分析方法及数据类型。

表1
这里遇到两个问题:
一是,在数据类型中,为什么有的RCT是个体参与者数据IPD,有的是聚合数据(Aggregate-Level Data,AgD)呢?基于商业角度,药厂或研究者,只能拿到自己研发的药物(如A药)的个体数据,而对方药厂研发药物(如B药)的个体数据只有监管机构如FDA可以得到,公众只能获得已发表的整体样本的汇总数据AgD。因此,拿不到所有比较药物的IPD,便催生了各大药厂针对同一类型药物展开间接比较研究。
二是,Anchored MAIC和Non-Anchored MAIC主要区别在哪?在于研究类型和间接比较方法。Anchored MAIC是两个相同对照组的RCT进行间接比较;而Non-Anchored MAIC纳入的研究更灵活,更容易执行,但证据级别弱于Anchored MAIC。它包括以下组合:
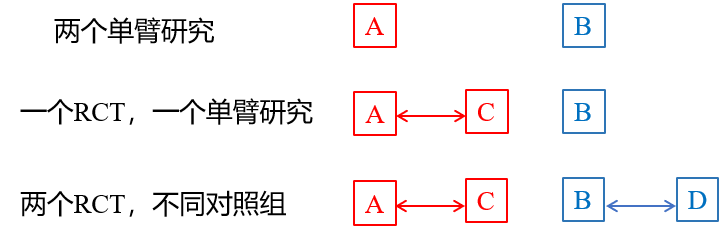
图2
例如今年的ASCO大会上,报告了两项间接比较研究的结果,满足了上述研究类型和数据类型:
1)采用Anchored MAIC法,比较乳腺癌靶向药Ribocicilib(MONALEESA-2)和Abemacicilib(MONARCH 3)的研究,该研究满足以下类型:
a)研究类型:两药研究都是RCT,有相同的对照组;
b)数据类型:Ribo有IPD,Abema有AgD;
2)采用Non-Anchored MAIC法,比较非小细胞肺癌药物Mobocertinib和Amivantamab的研究,该研究满足以下类型:
a)研究类型:两药都是单臂试验,没有共同对照组;
b)数据类型:Mobo有IPD,Ami有AgD。

图3
总结
1)做MAIC的研究类型是
a) Anchored MAIC—2个RCT且有共同对照组;
b) Non-anchored MAIC—2个研究(单臂,RCT,没有共同对照组,都可)。
2)做MAIC的数据类型是:两项研究一个有IPD,一个有AgD
此外,ASCO的两个研究在采用Anchored MAIC/Non-anchored MAIC之前均做了匹配和加权,那是为什么呢?
Q3
间接比较的前提什么?
首先,纳入的RCT或研究之间具有相似性。相似性包括,研究设计、纳入人群、评价方法、终点指标等。两药Ribo(MONALEESA-2)和Abema(MONARCH 3)使用相同的对照组,但患者基线在种族、既往化疗、既往内分泌治疗、脑转移患者等方面明显不同,因此不具备可比性。故间接比较第一步是matching(匹配),将Ribo药IPD的入排标准与Abema药AgD进行匹配,达到相似性。匹配的过程中,拥有IPD的样本,样本量会减少。见下表2。
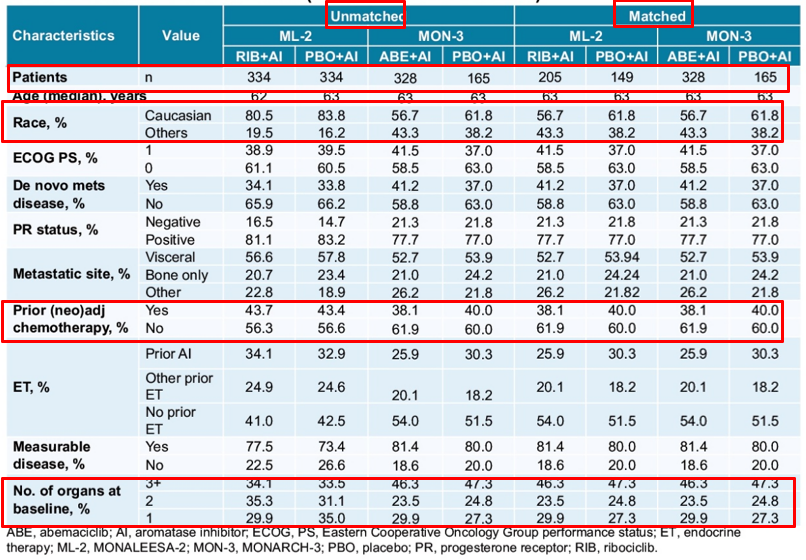
表2
但是,即使人群特征及疾病状态相似,但基线特征的分布差异过大,间接比较仍然不可靠。所以,第二步是weighting(加权),使用Logistic或Cox回归等方法调整Ribo个体数据的权重,使得两药基线特征分布基本相同,重建Ribo的IPD,与Abema进行间接比较,得到调整后的Adjusted Hazzard Ratio(95%CI)。匹配调整后的结果,就好像把两药放在同一患者群里做试验一样。这就是图1-(3)提到的,临床试验常见的间接比较方法——匹配调整间接比较(MAIC)。下图4展示了Non-Anchored MAIC匹配调整的过程。

图4
总结
间接比较的前提是
1) 匹配:将IPD研究的入排与AgD研究的入排匹配一致,过程中IPD研究样本量会减少;
2) 调整/加权:使用回归模型,将IPD研究基线分布的权重,调整到与AgD研究一致,重建IPD研究的Adjusted Hazzard Ratio(95%CI)。
匹配调整重建IPD,重新计算Adjusted OS、PFS、HR…后,终于可以做间接比较了,那么就剩最后一个问题。
Q4
如何做间接比较?
Anchored MAIC法比较A与B,C是共同对照。那么A与B是如何借助C,计算比较的呢?举个例子,已知A比C高20cm,B比C高10cm,那么可得A比B高10cm。统计抽样中除了比较A与B差异大小外,还要考虑随机误差,才能分析间接比较结果的差异是否有统计学意义。因为用于间接比较的两个RCT分别是独立的研究,故间接比较的方差等于两个RCT方差之和,即Bucher法。
一图读懂Bucher法(因为我们无法获知上述研究的IPD,故HR使用了模拟数据来计算):
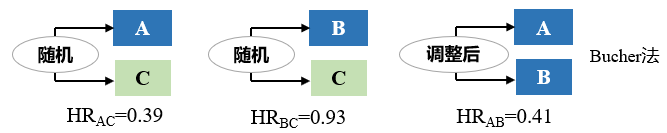
图5
临床试验终点比较常采用比值比(odds ratio, OR)、风险比(hazard ratio, HR)等。如图2中HR值,可先计算各组的HRAC及HRBC,再计算HRAC/HRBC,就可得到A与B间接比较的HRAB。因构建置信区间要保证残差服从正态分布,故需对HR及标准差取对数后相减/相加。
小结
最后,借上述案例,小结一下Anchored MAIC的分析过程:

Non-anchored MAIC则不适用Bucher法,而是使用新建IPD计算的Adjusted HR与AgD研究HR放在KM曲线中,直接比较。
最后,对于MAIC间接比较方法研究结果的解读需谨慎。当两项研究在基线方面不匹配因素众多,可能使比较结果存在偏倚。RCT研究才是检验药物疗效的金标准。
但如果同类型的药物不止A,B两种,有三种及以上;比如在A,B,C,D…药中既有直接比较又有间接比较,或同时有多个间接比较(如:A vs. B可以通过AC和BC获得,亦可通过AD和BD获得),合并直接比较及间接比较结果的混合比较MTC,将提高结果的精确性和统计学效能,同时可以综合评价多种药物并排序,筛选出最佳药物,于是2002年Lumley等提出了网状meta分析NMA,拓展了间接比较的框架,具体情况请见下回文章分析。
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)