2023-04-17

《联合用药研究实操训练营》上期课程,选用的案例是辉瑞的PALOMA研究,邀请中国医学科学院肿瘤医院主任马飞教授、美国西北大学Feinberg医学院张晖教授、美国圣路易斯华盛顿大学刘磊教授、美国杜克大学医学中心罗晟教授,共同探讨PALOMA研究阴性数据背后的原因,启发新的科研思路,通过对RCT研究的原始数据进行二次分析,发表一些高质量的文章(本推文最后附:使用PALOMA案例数据,通过二次分析,成功发表的文章列表)。
1、PALOMA研究的背景介绍。
2、乳癌临床专家从医学角度分析PALOMA-2研究OS阴性结果的原因。
3、统计专家从统计角度分析和解答该研究阴性结果的可能原因。
4、如果删失数据(即数据缺失),有哪些可靠的处理方法?
5、该研究进行亚组分析如何考量,探索未来研究可能的获益人群?
6、独立数据委员会(BICR)和研究者(INV)评估RCT研究中的无进展生存率出现差异,如何选择?
7、采用Cox比例风险模型进行生存分析,生存曲线发生交叉,如何采用正确的统计分析方法?
8、真实世界研究中采用sIPTW vs PSM有哪些优缺点?
9、怎样按照国际ICH指南对联合用药研究提供合理性依据?
10、联合用药的剂量的安全性探索,如何选择爬坡,降坡,还是safety run in 设计?
11、如何选择联合用药最优的药物组合(药物机理是基础)?
12、联合用药研究析因分析设计需要避免的错误。
案例讨论:
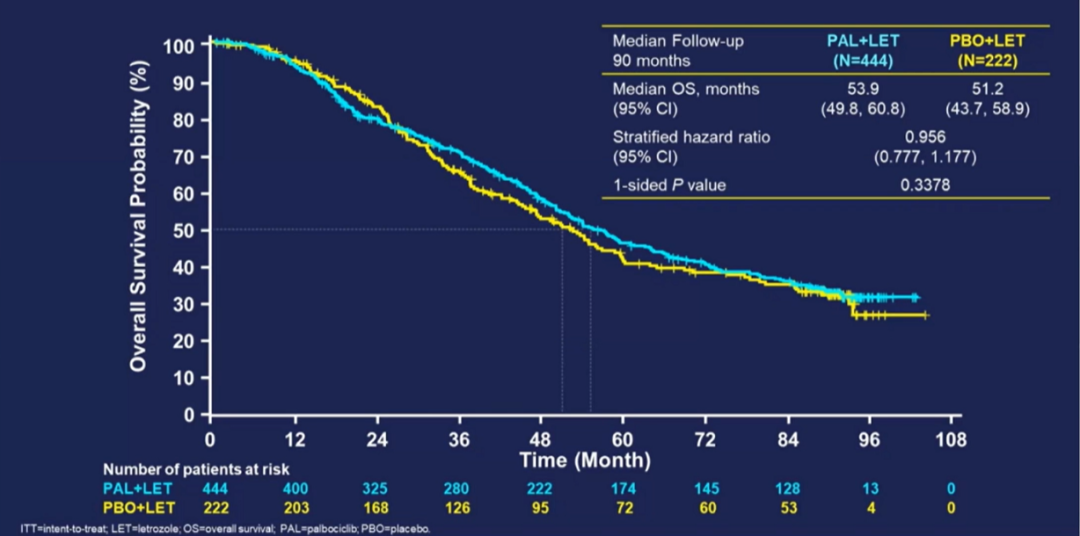
2022年ASCO公布的PALOMA-2总生存结果显示:中位随访90个月后(数据截止2021年11月15日),总生存事件数为405(占总体60.8%);有相当比例的患者无法进行随访(撤回知情同意书同或失访)导致数据删失;治疗组的删失比例为13%,PAL+LET组和PBO+LET组的中位OS分别为53.9个月(95% CI:49.8-60.8)和51.2个月(95% CI:43.7-58.9)(HR=0.956;95% CI:0.777-1.177;单侧P=0.3378)。PAL+LET组对比PBO+LET组,总生存期在一定程度的延长,但未达到统计学差异(绝对差异2.7个月)。
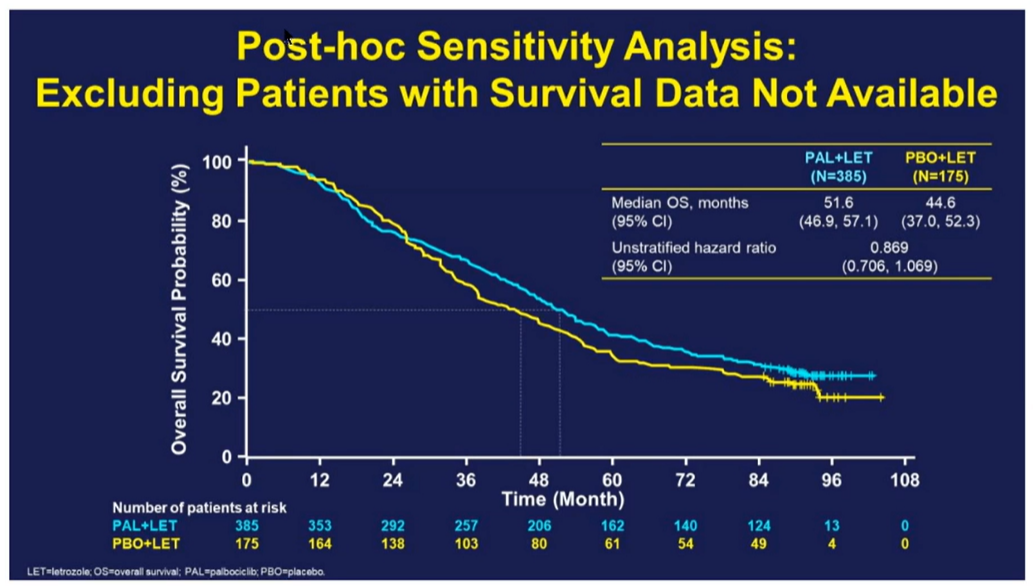
辉瑞将影响OS最终获益的原因归结于“missing data”。为了证明OS的疗效不止2.7个月的差异,辉瑞又做了删除missing data后的敏感性分析,结果显示:PAL+LET组和PBO+LET组的中位OS(95% CI)分别为51.6个月(46.9-57.1)和44.6个月(37.0-52.3)(HR=0.869;95% CI:0.706-1.069),绝对差异7个月。
对于辉瑞的这次事后敏感性分析,有没有实际意义?其分析结果是否有参考价值,从而影响FDA对研究结果的判断?听听导师们的观点:
实操练习:
独立数据委员会(BICR)和研究者(INV)评估的无进展生存率存在差异时,如何选择?

PALOMA-2:一项全球、III期、双盲、安慰剂对照随机临床研究,证实了palbociclib做为绝经后雌激素受体阳性(ER+),人表皮生长因子受体2(HER2-)阴性转移性乳腺癌患者初始治疗的临床获益。与来曲唑+安慰剂治疗相比,palbociclib与来曲唑联合使用延长了这部分患者的无进展生存期(PFS),长达至少10个月,有力验证了与之相似设计的II期PALOMA-1研究的结果。
这个研究的PFS结果非常惊艳,图A显示了研究者评估的意向治疗人群的无进展生存率(初步分析);Palbociclib-Letrozole组444名患者的中位无进展生存期为24.8个月(95%CI,22.1-无法估计),安慰剂-Letrozole组222名患者中位无进步生存期为14.5个月(95% CI,12.9-17.1)。
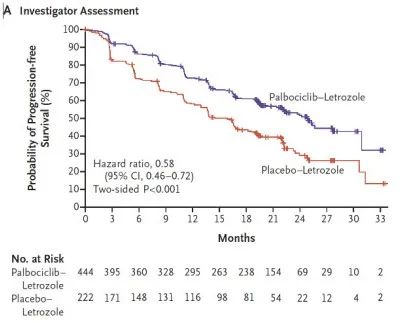
图A
图B显示了意向治疗人群的无进展生存率,通过独立数据委员会进行评估;Palbociclib-Letrozole组444名患者的中位无进展生存期为30.5个月(95%CI,24.7-不可估计),安慰剂-Letrozole组222名患者中的中位生存期为19.3个月。
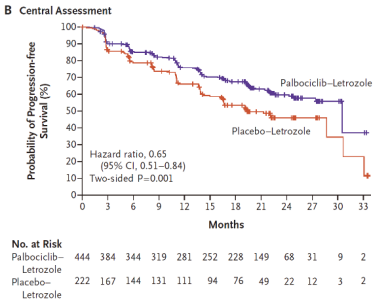
图B
INV和BICR都得出了一致的结果,即:Palbociclib联合Letrozole能改善患者无进展生存率。但是研究结果有微小差异:INV得出的HR 0.58(95% CI 0.46-0.72),而BICR HR 0.65(95% CI 0.51-0.84)。
辉瑞公司没有约定在独立数据委员会(BICR)评估的PFS和研究者(INV)评估的PFS中,以哪一个作为主要终点,临床医生和统计专家的观点各有不同,中国医学科学院肿瘤医院主任马飞教授、美国西北大学Feinberg医学院张晖教授、美国圣路易斯华盛顿大学刘磊教授、美国杜克大学医学中心罗晟教授参与了讨论:
马飞教授:在临床上这种情况非常常见,尤其是在早期BICR还不是那么成熟的时候,两者的结果差距会更大,作为一名临床医生,我们更倾向于选择INV的结果,因为INV能结合临床资料(患者的主诉、生活质量等方面)综合评估PFS,这可能更接近于真实情况,而监管机构可能会认为INV会带有主观意识判定患者现状,所以会综合BICR的结果,但是BICR只能通过现有的文书资料确定PFS。
张晖教授:我同意马飞教授的观点,INV具备更全面的临床知识,对于疾病把控更全面。另外从统计学家角度看,INV得出的95% CI范围0.26,而BICR得出的95% CI范围0.33,单从INV获得的95% CI范围更小来看可能INV获得的数据更具备统计学可靠性。
刘磊教授:我也同意两位教授的观点。另外我们看BICR获得的KM图,超过50% PFS rate的对照组和实验组几乎就没有事件发生,后续没有足够的事件数目来支撑我们获得50% PFS rate。
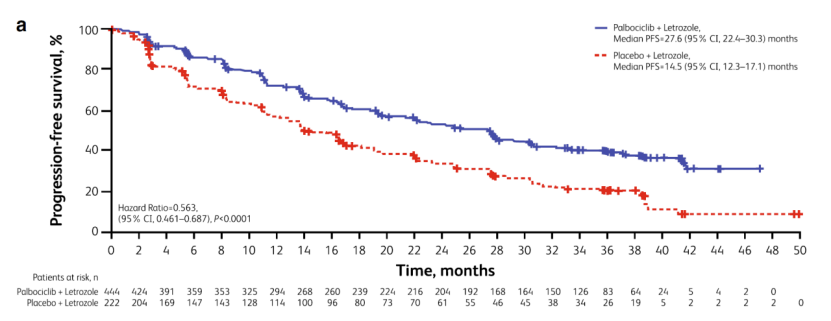
罗晟教授:我可能更偏向选择BICR,因为潜在偏倚会少很多。关于刘教授提到的50% PFS rate,我觉得可能是因为随访时间较短的原因,后续如果延长随访时间,可能这个问题就会迎刃而解。我们进一步看看该研究最后呈现的生存曲线结果,我们发现延长随访时间,就解决了刚才提到50% PFS rate事件数较少的问题。

希望深度学习《联合用药研究实操训练营》的学员,可扫描二维码课程咨询


添加小编微信

百度浏览 来源 : 国际临研
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。




发表评论
注册或登后即可发表评论
登录注册
全部评论(0)