2023-09-11 来源 : VIP说
前段时间闹得沸沸扬扬的罗氏SKYSCRAPER-01研究“数据泄露”一事想必大家都知道了,由于内部人员的错误操作,“不小心”将TIGIT单抗Tiragolumab正在进行的III期SKYSCRAPER-01研究的中期数据挂到了罗氏官网上。
这次的不小心,让大家看到了SKYSCRAPER-01研究第二次中期分析的OS结果,Tiragolumab联合阿替利珠单抗组的mOS 估计为 22.9 个月,阿替利珠单抗单药治疗组的mOS 估计为 16.7 个月,风险比为 0.81,OS置信区间上限为1.03已过1,p值为 0.081,未超过统计显著性的典型阈值 0.05。从无意间披露的数据来看,TIGIT联合阿替利珠单抗目前尚未能显著延长PD-L1高表达NSCLC患者的生存。(找回这张删除的图费了很大功夫)
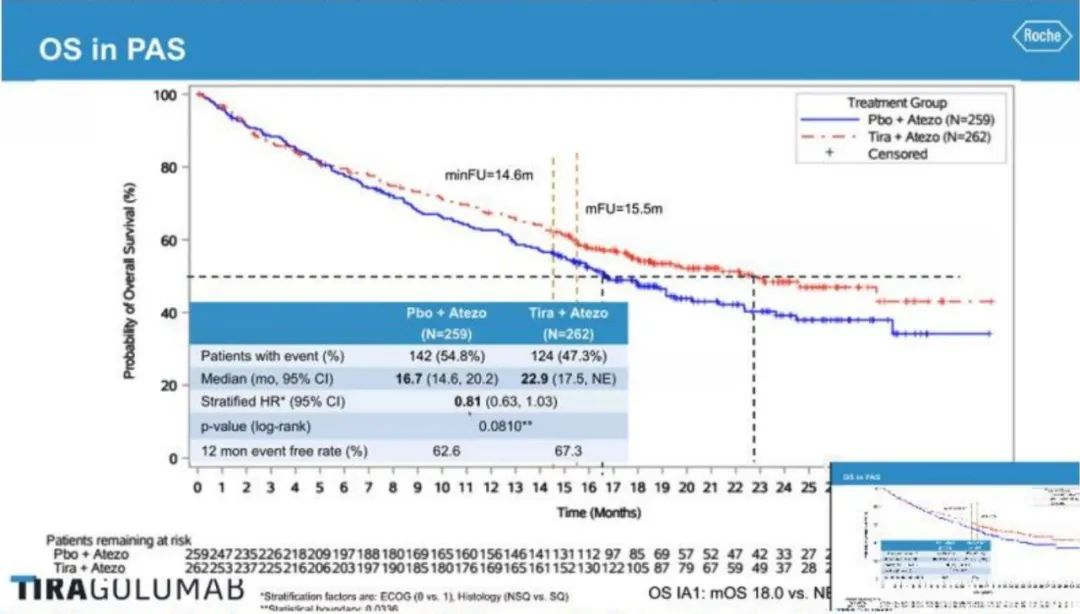
而在一年前的5月10日,罗氏公布了SKYSCRAPER-01研究第一次中期分析结果,Tiragolumab联合阿替利珠单抗错失了该研究第一个共同主要研究终点PFS,相较阿替利珠单抗单药治疗PD-L1高表达NSCLC未能延长PFS。仅仅一个月后的2022ASCO大会上,Tiragolumab联合阿替利珠单抗一线治疗广泛期SCLC的III期研究SKYSCRAPER-02结果公布,联合治疗无论在PFS还是OS上,与阿替利珠单抗联合化疗相比,均未能取得显著的改善。这给当下如火如荼开展中的TIGIT靶点开发,无疑当头泼上了一盆冷水。
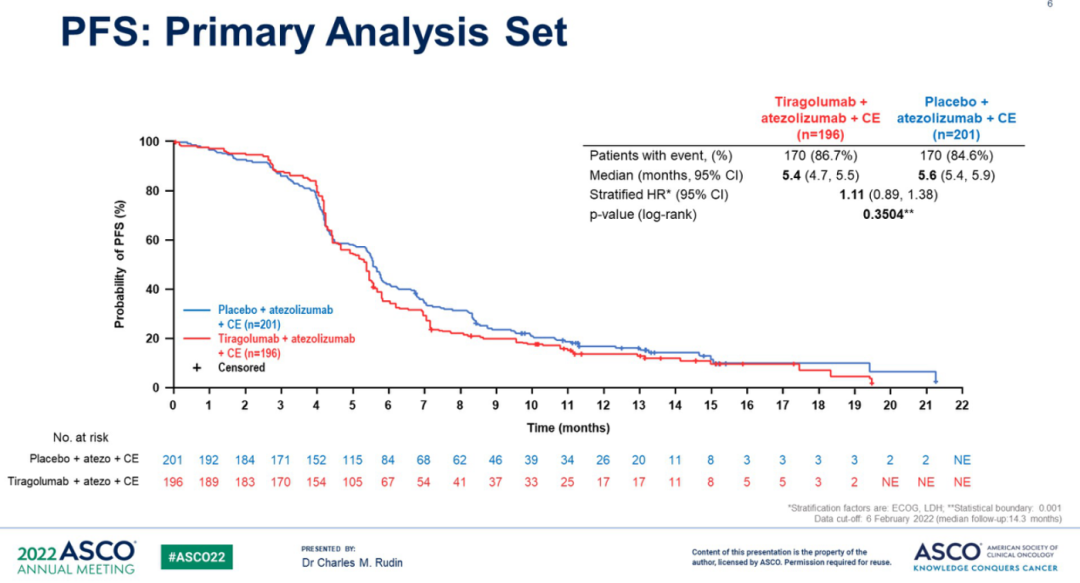
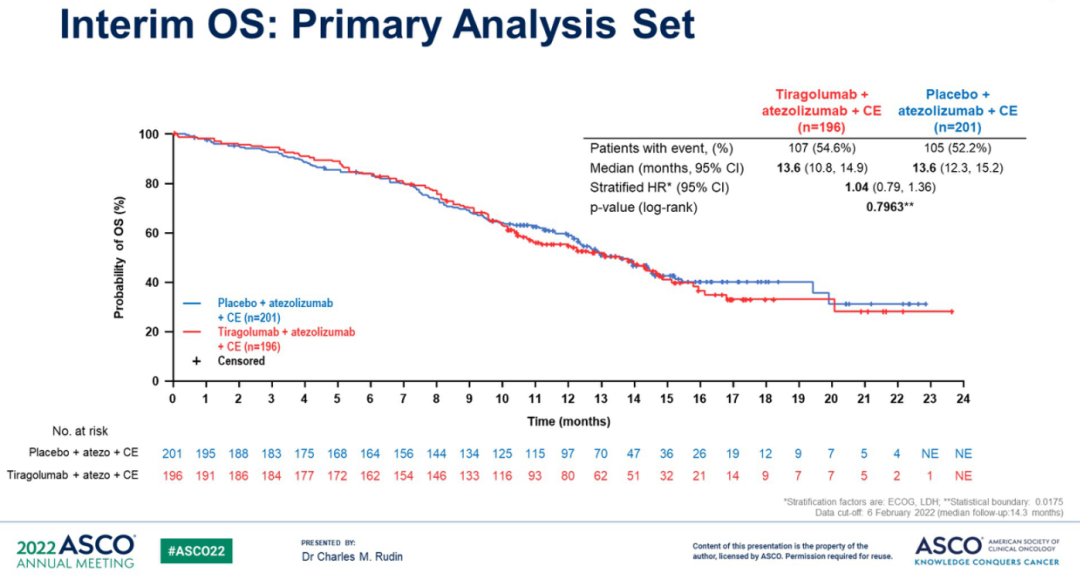
SKYSCRAPER-02研究PFS和OS
如何看待这次SKYSCRAPER-01研究不小心公布的OS结果呢?
我们都知道,IMpower-110研究显示,阿替利珠单抗单药一线治疗PD-L1≥50% NSCLC的mOS就已经达到了20.2个月(对照组14.7个月),回头看SKYSCRAPER-01这次公布的mOS为22.9个月[1],也就是说阿替利珠单抗联合TIGIT抗体相比阿替利珠单抗单药治疗仅延长了2个月左右的OS(虽然非头对头研究不能直接比,但有一定启示)。KEYNONTE-024研究中,帕博利珠单抗单药一线治疗PD-L1≥50% NSCLC的mOS也达到了26.3个月[6]。想来TIGIT单抗若上市价格不会低,那么加入TIGIT联合治疗mOS 22.9个月,对于PD-L1高表达NSCLC患者的价值究竟有多大呢?
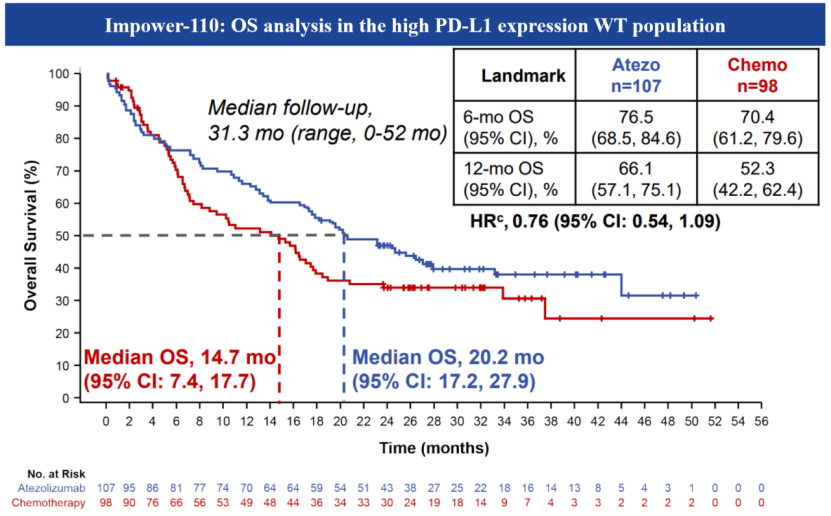

不是所有的PD-1都能延长OS
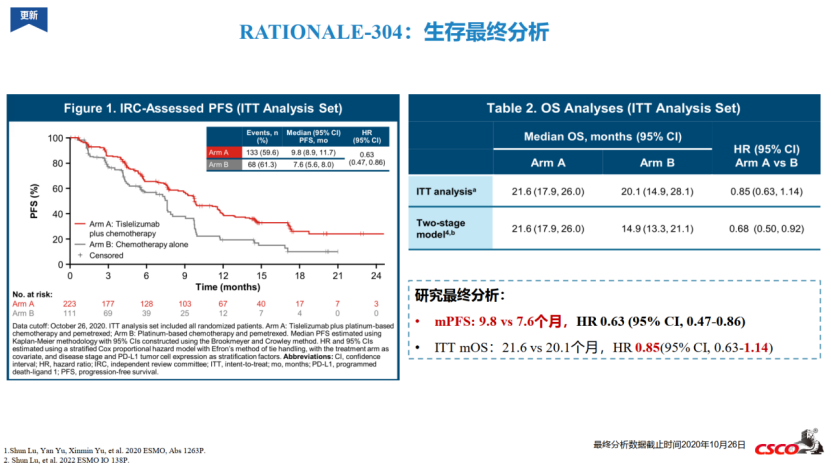
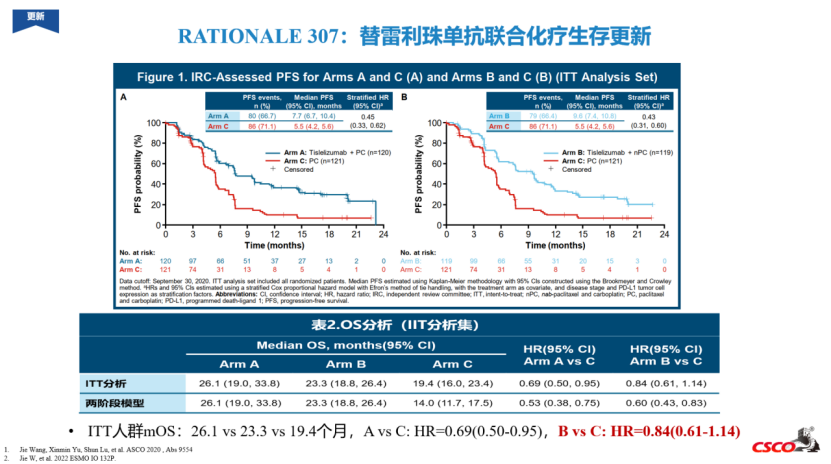
据悉,替雷利珠单抗联合TIGIT单抗的研究也在开展中,若仍然没有显著延长OS,无疑又是一盆凉水。
唯一OS双阳性的国产PD-1
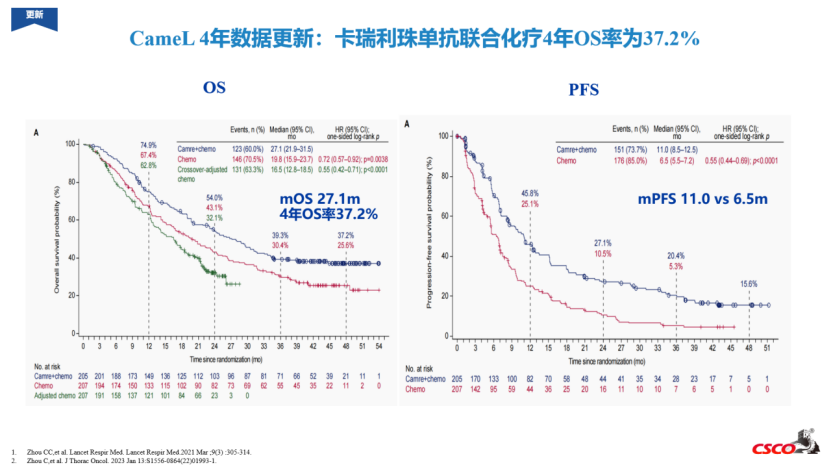

结语
参考文献:
[1] IMpower110: updated OS analysis of atezolizumab vs platinum-based chemotherapy as first-line treatment in PD-L1–selected NSCLC. 2020WCLC
[2] Shun Lu, et al. 2022 ESMO IO. 138P
[3] Wang J, et al. JAMA Oncol 2021 May 01;7(5)
[4] Zhou C et al. J Thorac Oncol 2023 May;18(5)
[5] Zhou C, et al. 2021ELCC. Abstract 960
[6] Martin Reck, et al. J Clin Oncol 39:2339-2349
版权声明:本网站所有注明来源“医微客”的文字、图片和音视频资料,版权均属于医微客所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源:”医微客”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,转载仅作观点分享,版权归原作者所有。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 本站拥有对此声明的最终解释权。





发表评论
注册或登后即可发表评论
登录注册
全部评论(0)